题目内容
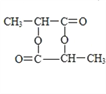
【题目】在烷烃分子中的基团:CH3—、—CH2—、![]() 中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。
中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示。
例如: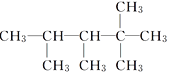 分子中,n1=6,n2=0,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
分子中,n1=6,n2=0,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子数为A,A与n1、n2、n3、n4的关系是:A=________,或A=________。
(2)四种碳原子数之间的关系为n1=________。
(3)若某烷烃分子中n2=n3=n4=1,写出该分子的结构简式和键线式,并对其进行命名:___________________。
【答案】3n1+2n2+n3 2(n1+n2+n3+n4)+2n3+2n4+2
![]() 2,2,3-三甲基戊烷;
2,2,3-三甲基戊烷;

![]() 2,3,3-三甲基戊烷;
2,3,3-三甲基戊烷;

![]() 2,2,4-三甲基戊烷
2,2,4-三甲基戊烷
【解析】
(1)由题知,伯、仲、叔、季碳原子上分别连有H原子个数为3、2、1,0故A=3n1+2n2+n3;又由烷烃的通式CnH2n+2中氢原子个数与碳原子个数之间的关系可写出:A=2nc+2=2(n1+n2+n3+n4)+2;
(2)因为3n1+2n2+n3=2(n1+n2+n3+n4)+2,故n1=n3+2n4+2;
(3)该烷烃分子中含有一个仲碳原子、一个叔碳原子、一个季碳原子,由第(2)小题可知,伯碳原子数(—CH3)为5个,由于—CH3只能连在链端,而不能夹在中间,所以只需将 进行组合连接,然后再补上—CH3即可。
进行组合连接,然后再补上—CH3即可。
因为伯、仲、叔、季碳原子结合的H原子分别为3、2、1、0个,所以根据伯、仲、叔碳原子数即可确定烷烃分子中H原子数为3n1+2n2+n3;根据烷烃的分子通式为CnH2n+2,n=n1+n2+n3+n4,即可确定烷烃分子中的H原子数为2(n1+n2+n3+n4)+2。
故答案为: 3n1+2n2+n3;2(n1+n2+n3+n4)+2 ;
由(1)中H原子数的关系可得3n1+2n2+n3=2(n1+n2+n3+n4)+2,整理即得n1=n3+2n4+2 。
故答案为:n3+2n4+2;
(3)依题意,分别将三个基团![]() 变换位置,写出共三种结构简式,然后按主链碳最多、支链数之和最小,相同基团合并命名的规则给予命名。
变换位置,写出共三种结构简式,然后按主链碳最多、支链数之和最小,相同基团合并命名的规则给予命名。
故答案为:
![]() 2,2,3-三甲基戊烷;
2,2,3-三甲基戊烷;

![]() 2,3,3-三甲基戊烷;
2,3,3-三甲基戊烷;

![]() 2,2,4-三甲基戊烷。
2,2,4-三甲基戊烷。

 科学实验活动册系列答案
科学实验活动册系列答案【题目】根据题意完成下列问题:
(1)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g) ![]() CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:_______________________________________。
(2)随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NO x、SO2、CO等大气污染气体的处理具有重要意义。用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)![]() N2(g)+CO2(g)。某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①则从反应开始到20mi时,以NO表示的平均反应速率= ________,该温度下该反应的平衡常数K=____(保留两位小数)
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是_____(写一条即可)。
③下列描述中能说明上述反应已达平衡的是__________;
A、容器内气体的平均摩尔质量保持不变
B、2v(NO)正=v(N2)逆
C、容器中气体的压强保持不变
D、单位时间内生成nmolCO2的同时生成2nmolNO
(3)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42-, 而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为_______________
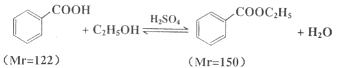
(4)有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料。

若A为SO2,B为O2,C为H2SO4,则负极反应式为_______________________________,电池总反应式为________________________。
【题目】根据要求回答下列问题:
(1)用大理石和100ml某稀盐酸反应制CO2 ,产生CO2的体积与反应时间的关系如图所示,其中产生CO2速率最快的为____段(选填“OE”、“EF”或“FG”),若该段内生成标准状况下的CO2 448mL,所用时间为2min,该段时间内用HCl来表示其反应速率,则速率为_____,(忽略反应后溶液体积的变化),若要使该反应的反应速率加快,下列措施可行的是______(填字母)。
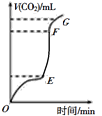
A.将大理石换用碳酸钙粉末 B.加入K2SO4溶液 C.升高温度
D.加入NaCl固体 E.增大盐酸的浓度
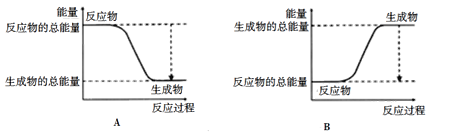
(2)对于反应2A2+B2=2A2B,已知A2、B2、A2B的键能如下表:
化学键 | A-A | B=B | A-B |
键能/kJ/mol | 236 | 406 | 163 |
下图能正确表示该反应过程中能量变化的选项是_______(填字母)。