题目内容
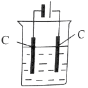
【题目】(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是 ;
②C组物质与水反应的离子方程式为 ;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有 (填化学式)。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是 → 。
②写出该反应的化学方程式,并标出电子转移的方向和数目____________。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
④H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是____________。
【答案】(1)①与水反应是否是氧化还原反应;
②2Na+2H2O=2Na++2OH-+H2↑;
③Cl2、Na2O2;
(2)①H2CrO4 Cr(OH)3
②2H2CrO4+3H2O2 = 3O2↑+2H2O+2Cr(OH)3
③3.36L
④H2O2作氧化剂,其还原产物是H2O;H2O没有毒性及污染性;
【解析】
试题分析:(1)①上述分类中,A组的物质与水反应,元素的化合价都没有发生变化,B组中元素的化合价发生了变化。因此分成A、B两组的依据是与水反应是否是氧化还原反应;
②在C组的物质中,与水发生反应,水只作氧化剂的是Na,Na与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑;
③D组物质Cl2、Na2O2、NO2与水反应中,水即不作氧化剂,也不作还原剂,反应的方程式是:Cl2+H2O= HCl+HClO;该反应中氧化剂和还原剂物质的量之比为1∶1,符合题意;2Na2O2+2H2O=4NaOH+O2↑;该反应中氧化剂和还原剂物质的量之比为1∶1,符合题意;3NO2+H2O=2HNO3+NO,该反应中氧化剂和还原剂物质的量之比为1∶2,不符合题意,因此氧化剂和还原剂物质的量之比为1∶1的物质有Cl2、Na2O2;(2)①H2O2→O2的过程中,氧元素的化合价由-1价升到了0价,所以H2O2是还原剂,H2CrO4为氧化剂,发生还原反应H2CrO4→Cr(OH)3;
②根据电子得失守恒可知配平方程式为2H2CrO4+3H2O2 = 3O2↑+2H2O+2Cr(OH)3;
③根据以上分析可知还原剂失去的电子总数为6e-,氧化剂得到的电子总数为6e-,所以电子的转移数目为6e-,反应转移了6mol电子生成3mol氧气,如反应转移了0.3mol电子,则会生成0.15mol即3.36L氧气;
④H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是H2O2作氧化剂,其还原产物是H2O;H2O没有毒性及污染性。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案