题目内容
9.写出下列反应的化学方程式,并指出反应类型:(1)用甲苯制备TNT
 ,取代反应
,取代反应(2)苯酚和浓溴水的反应
 ,取代反应
,取代反应(3)1,2-二溴乙烷与足量氢氧化钠的乙醇溶液加热:CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaBr+2H2O,消去反应
(4)2-丙醇与氧气在催化剂作用下反应2CH3CH(OH)CH3+O2$→_{△}^{Cu/Ag}$2CH3COCH3+2H2O,氧化反应.
分析 (1)甲苯和浓硝酸在浓硫酸催化剂作用下发生取代反应生成三硝基甲苯和水;
(2)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代;
(3)1,2-二溴乙烷和氢氧化钠的乙醇溶液共热发生消去反应生成乙炔和溴化钠、水;
(4)2-丙醇与氧气在铜催化作用下反应,醇羟基和醇羟基相连的碳分别脱氢生成酮;
解答 解:(1)甲苯可以和浓硝酸之间发生取代反应生成2,4,6-三硝基甲苯,即TNT,化学反应方程式为: ,属于取代反应;
,属于取代反应;
故答案为: ;取代反应;
;取代反应;
(2)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代反应的化学方程式为: ,反应类型为取代反应;
,反应类型为取代反应;
故答案为: ;取代反应;
;取代反应;
(3)1,2-二溴乙烷和氢氧化钠的乙醇溶液共热发生消去反应,反应的化学方程式为:CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaBr+2H2O,
故答案为:CH2BrCH2Br+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaBr+2H2O,消去反应;
(4)2-丙醇与氧气在铜催化作用下发生氧化反应,反应生成丙酮,反应的方程式为:2CH3CH(OH)CH3+O2$→_{△}^{Cu/Ag}$2CH3COCH3+2H2O,
故答案为:2CH3CH(OH)CH3+O2$→_{△}^{Cu/Ag}$2CH3COCH3+2H2O,氧化反应.
点评 本题考查了方程式的书写,根据反应物、生成物和反应条件书写方程式,明确发生的化学反应原理是解答本题的关键,注意常见有机物的性质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.如图所示,在较高温度时,钾、氧两元素形成的一种晶体结构与NaCl晶体结构相似,则该化合物的化学式为( )


| A. | KO2 | B. | K2O2 | C. | K2O3 | D. | K2O |
20.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑.
(2)实验①的目的是研究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中 | 试管A中不再产生气泡 试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 试管A、B中均未见气泡产生 |
(2)实验①的目的是研究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
4.下列关于乙烯的说法不正确的是( )
| A. | 分子中含有碳碳双键 | B. | 可作水果催熟剂 | ||
| C. | 分子式为C2H6 | D. | 能使溴水褪色 |
1.下列物质的说法错误的是( )
| A. | 某实验过程中得到一定量的碘水,可用裂化汽油从碘水中萃取出碘 | |
| B. | 芳香烃主要来自于煤焦油和石油化工中的催化重整 | |
| C. | 常压分馏得到的汽油是混合物,没有固定的沸点 | |
| D. | 乙烯是轻质油裂解的产物,其产量可用来衡量一个国家的石油化工发展水平 |
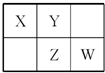 四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.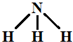 (写结构式);
(写结构式); ;
;