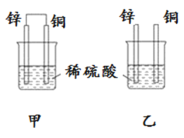
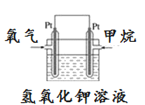
题目内容
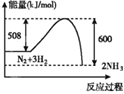
【题目】已知:2H2(g)+O2(g)=2H2O(g)反应放出的热量为483.6 kJ。有关键能数据如表所示:则水分子中O—H键键能为( )
化学键 | H-H | O=O |
键能/(kJ·mol-1) | 436 | 498 |
A.463.4 kJ·mol-1B.926.8 kJ·mol-1C.221.6 kJ·mol-1D.413 kJ·mol-1
【答案】A
【解析】
2mol氢气和1mol氧气反应生成2mol水时,断裂反应物分子间的化学键吸收的热量为2×436kJ+498kJ=1370kJ,反应放出的热量为483.6 kJ,所以形成2molH2O放出的热量为483.6 kJ+1370kJ=1853.6kJ,所以形成1molO—H键放出的热量为![]() =463.4 kJ,则水分子中O—H键键能为463.4 kJ·mol-1,故选A。
=463.4 kJ,则水分子中O—H键键能为463.4 kJ·mol-1,故选A。

练习册系列答案
相关题目