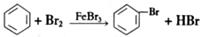��Ŀ����
��12�֣�ij��ɫ����Һ�п��ܴ��ڴ���Ag����Mg2����K����Cu2���е�һ�ֻ��֣�����д���пհס�
��1���������κ�ʵ��Ϳ��Կ϶���Һ�в����ڵ�������________________��
��2��ȡ����ԭ��Һ���������ϡ���ᣬ�а�ɫ�������ɣ��ټ������ϡ���ᣬ��������ʧ��˵��ԭ��Һ�п϶����ڵ�������________����Ӧ�����ӷ���ʽΪ_______________��
��3��ȡ��2������Һ�ӹ�����NaOH��Һ�����ְ�ɫ������˵��ԭ��Һ�п϶���________���йط�Ӧ�����ӷ���ʽΪ________________��
��4��ԭ��Һ�п��ܴ������ڵ���������
��1���������κ�ʵ��Ϳ��Կ϶���Һ�в����ڵ�������________________��
��2��ȡ����ԭ��Һ���������ϡ���ᣬ�а�ɫ�������ɣ��ټ������ϡ���ᣬ��������ʧ��˵��ԭ��Һ�п϶����ڵ�������________����Ӧ�����ӷ���ʽΪ_______________��
��3��ȡ��2������Һ�ӹ�����NaOH��Һ�����ְ�ɫ������˵��ԭ��Һ�п϶���________���йط�Ӧ�����ӷ���ʽΪ________________��
��4��ԭ��Һ�п��ܴ������ڵ���������
| A��Cl�� | B��NO3�� | C��CO3 2�� | D��OH�� |
����12�֣�
��1��Cu2����
��2��Ag+��Ag++Cl��=AgCl��
��3��Mg2+��Mg2++2OH��= Mg(OH)2��
��4��B ����ѡ���÷֣�
��1��Cu2����
��2��Ag+��Ag++Cl��=AgCl��
��3��Mg2+��Mg2++2OH��= Mg(OH)2��
��4��B ����ѡ���÷֣�
�����������1�������д���Cu2������Һ����ɫ������ɫ��Һ��һ��������Cu2������2����Cl����Ag+��Ӧ�����ɰ�ɫ��AgCl������������ˮ��ϡ���ᣬ��ʵ�飨2��˵��ԭ��Һ�п϶�����Ag+��ԭ����Ag++Cl��=AgCl������3��������ϡ���������ʵ�飨2��������Һ����Ag+��OH������H+��Ӧ������ˮ��OH������Mg2+��Ӧ�����ɰ�ɫ��Mg(OH)2��������ʵ�飨3��˵��ԭ��Һ�п϶���Mg2+���йط�ӦΪOH��+H+= H2O��Mg2++2OH��= Mg(OH)2������4����Cl����Ag+��Ӧ����ԭ��Һ�����ܺ��д�����Cl����A�����NO3����Ag+��Mg2+�����ܷ�Ӧ�������������ˮ���ɣ�B����ȷ��CO3 2����Ag+��Mg2+���ܷ�Ӧ�����ɰ�ɫ������C�����OH����Ag+��Mg2+���ܷ�Ӧ�����ɰ�ɫ������D�����

��ϰ��ϵ�д�
 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
�����Ŀ
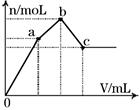
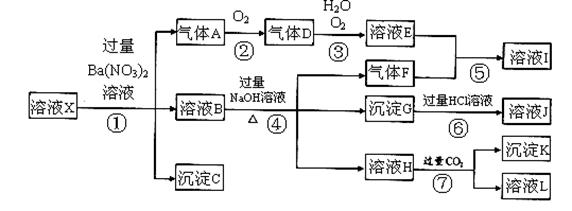

 Mg2+(aq) +2NH3��H2O(aq)
Mg2+(aq) +2NH3��H2O(aq)