题目内容
6.下列关于金属元素特征的叙述正确的是( )①金属元素的原子只有还原性,离子只有氧化性;
②金属元素在化合物中一般显正价;
③金属性越强的元素相应的离子氧化性一般越弱;
④金属元素只有金属性,没有非金属性;
⑤最外层电子数越多的金属原子,金属性越强;
⑥离子化合物一定含金属元素.
| A. | ①②③ | B. | ②③ | C. | ①⑤⑥ | D. | 全部 |
分析 金属元素的化合价一定是正价,因而其原子只有还原性,但其离子不一定只有氧化性,如Fe2+就有还原性,金属元素难以得到电子,在化学反应中只能失去电子,金属性越强的元素相应的离子氧化性越弱,在金属和非金属分界线附近的金属一般具有金属性和非金属性.
解答 解:①对于多价金属离子来说,较低价态的金属离子既有氧化性又有还原性,例Fe2+,Fe2++Zn=Fe+Zn2+,2Fe2++Cl2═2Fe3++2Cl-,故①错误;
②因为金属元素的原子只具有还原性,故在化合物中只显正价,故②正确;
③金属性越强的元素越易失去电子,单质的还原性越强,对应的离子越难以得电子,氧化性越弱,故③正确;
④金属性较弱的金属元素具有一定的非金属性,如在金属和非金属分界线附近的金属,故④错误.
⑤金属性强弱与失电子的多少无关,只与得失电子的难易程度有关,所以与最外层电子数无关,故⑤错误;
⑥离子化合物氯化铵中不含金属元素,故⑥错误;
故选B.
点评 本题考查金属的性质,题目难度中等,注意对于此类结论性判断,只要能举出相反的例子,即可证明叙述错误.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
16.下列有关物质结构与粒子间的作用方式的叙述中,正确的是( )
| A. | 化学键只存在于分子内,分子间作用力只存在于分子间 | |
| B. | 分子晶体在熔化时,共价键没有被破坏 | |
| C. | 在晶体里有阳离子存在时,不一定有阴离子存在 | |
| D. | 物质在溶于水的过程中,化学键一定会被破坏或改变 |
17.镁条和铝片为电极,并用导线连接同时插入NaOH溶液中,下列说法正确的是( )
| A. | 镁条作负极,电极反应:Mg-2e-=Mg2+ | |
| B. | 铝片作负极,电极反应:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 电流从Al电极沿导线流向Mg电极 | |
| D. | 铝片上有气泡产生 |
14.下列取代基或微粒中,碳原子都满足最外层为8电子结构的是( )
| A. | 苯 | B. | 乙基(-CH2CH3) | C. | 碳正离子[(CH3)3C+] | D. | 碳烯(:CH2) |
11. A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
请回答下列问题:
(1)Z的化学式为NO2.乙的结构式为N≡N.
(2)B的最高价氧化物的电子式为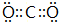 .
.
(3)用电子式表示A元素和E元素形成化合物的过程: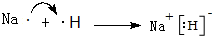 .
.
(4)G的单质与水反应的离子方程式Cl2+H2O?H++Cl-+HClO.
(5)F的单质与E的最高价氧化物的水化物反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(6)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.W空气燃料电池放电时负极反应式为N2H4+4OH--4e-=N2↑+4H2O.
 A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.| C | D | |
| G |
(1)Z的化学式为NO2.乙的结构式为N≡N.
(2)B的最高价氧化物的电子式为
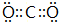 .
.(3)用电子式表示A元素和E元素形成化合物的过程:
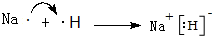 .
.(4)G的单质与水反应的离子方程式Cl2+H2O?H++Cl-+HClO.
(5)F的单质与E的最高价氧化物的水化物反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(6)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.W空气燃料电池放电时负极反应式为N2H4+4OH--4e-=N2↑+4H2O.
15.下列关于元素电负性大小的比较中,不正确的是( )
| A. | O<S<Se<Te | B. | C<N<O<F | C. | P<S<O<F | D. | K<Na<Mg<Al |
9.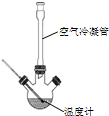 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
药品物理常数
填空:
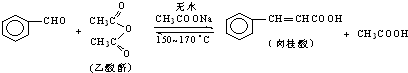
合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、苯甲醛和乙酸酐,振荡使之混合均匀. 在150~170℃加热1小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)该装置的加热方法是空气浴(或油浴).加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
(3)不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解.
粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
反应混合物$→_{碳酸钠溶液}^{加入饱和}$$→_{苯甲醛}^{蒸馏除去}$$\stackrel{盐酸酸化}{→}$$\stackrel{操作I}{→}$$→_{干燥}^{过滤、洗涤}$肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是冷却结晶;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是重结晶(均填操作名称).
(6)设计实验方案检验产品中是否含有苯甲醛取样,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛,或加入用新制氢氧化铜悬浊液,若出现砖红色沉淀,说明含有苯甲醛.
 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
药品物理常数
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、苯甲醛和乙酸酐,振荡使之混合均匀. 在150~170℃加热1小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)该装置的加热方法是空气浴(或油浴).加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
(3)不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解.
粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
反应混合物$→_{碳酸钠溶液}^{加入饱和}$$→_{苯甲醛}^{蒸馏除去}$$\stackrel{盐酸酸化}{→}$$\stackrel{操作I}{→}$$→_{干燥}^{过滤、洗涤}$肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是冷却结晶;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是重结晶(均填操作名称).
(6)设计实验方案检验产品中是否含有苯甲醛取样,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛,或加入用新制氢氧化铜悬浊液,若出现砖红色沉淀,说明含有苯甲醛.