题目内容
9.下列说法正确的是( )| A. | 只用一种试剂就可以鉴别甲苯、乙醇和四氯化碳 | |
| B. | 若两种烃中碳、氢元素的质量分数分别相同,它们必定是同系物 | |
| C. | CH3-CH=CH2分子中所有原子一定处于同一平面 | |
| D. | 某烷烃的命名为3,4,4-三甲基己烷 |
分析 A.甲苯、四氯化碳都不溶于水,二者密度不同,乙醇与水混溶;
B.如结构不同,则不是同系物;
C.含有甲基,具有甲烷的结构特点;
D.主链编号错误,支链序号之和应最小.
解答 解:A.甲苯、四氯化碳都不溶于水,二者密度不同,乙醇与水混溶,可加入溴水鉴别,故A正确;
B.若两种烃中碳、氢元素的质量分数分别相同,但如结构不同,则不是同系物,如乙烯和环丙烷,故B错误;
C.含有甲基,具有甲烷的四面体结构特点,原子不可能在同一个平面上,故C错误;
D.主链编号错误,支链序号之和应最小,应为3,3,4-三甲基己烷,故D错误.
故选A.
点评 本题考查较为综合,涉及有机物的结构、性质以及命名的综合考查,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
19.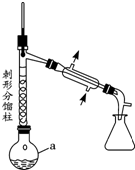 乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下: NH2+CH3COOH$\stackrel{△}{?}$
NH2+CH3COOH$\stackrel{△}{?}$ NHCOOCH3+HO
NHCOOCH3+HO
已知:
①苯胺易被氧化.
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
实验步骤如下:
步骤1:在a中,加入9mL (0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,依照如图装置组装仪器.
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全.
步骤3:趁热将反应混合物倒入盛有100mL 冷水的烧杯中,冷却后抽滤(一种快速过滤方法)、洗涤,得到粗产品.
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g.
请回答下列问题:
(1)仪器a的名称为圆底烧瓶,所选仪器a的最佳规格是B(填序号).
A.25mL B.50mL C.100mL D.250mL
(2)实验中加入少许锌粉的目的是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中,控制温度计读数在105℃左右的原因是温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出.
(4)判断反应已基本完全的方法为锥形瓶不再有水增加.
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是冷却后固体析出粘在瓶壁上不易处理.
(6)步骤4中粗产品进一步提纯,该提纯方法是重结晶.
(7)本次实验的产率为80%.
 乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下: NH2+CH3COOH$\stackrel{△}{?}$
NH2+CH3COOH$\stackrel{△}{?}$ NHCOOCH3+HO
NHCOOCH3+HO已知:
①苯胺易被氧化.
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| 乙酰苯胺 | 114.3℃ | 305℃ | 微溶于冷水、易溶于热水 |
| 苯胺 | -6℃ | 184.4℃ | 微溶于水 |
| 醋酸 | 16.6℃ | 118℃ | 易溶于水 |
步骤1:在a中,加入9mL (0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,依照如图装置组装仪器.
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全.
步骤3:趁热将反应混合物倒入盛有100mL 冷水的烧杯中,冷却后抽滤(一种快速过滤方法)、洗涤,得到粗产品.
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g.
请回答下列问题:
(1)仪器a的名称为圆底烧瓶,所选仪器a的最佳规格是B(填序号).
A.25mL B.50mL C.100mL D.250mL
(2)实验中加入少许锌粉的目的是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中,控制温度计读数在105℃左右的原因是温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出.
(4)判断反应已基本完全的方法为锥形瓶不再有水增加.
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是冷却后固体析出粘在瓶壁上不易处理.
(6)步骤4中粗产品进一步提纯,该提纯方法是重结晶.
(7)本次实验的产率为80%.
20.下列对一些实验事实的理论解释正确的是( )
| 选项 | 实 验 事 实 | 理 论 解 释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子半径小于氧原子 |
| B | 干冰的熔沸点低 | 干冰为分子晶体 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
17.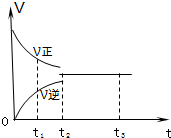 如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
 如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,只有正方向反应没有逆方向反应 | |
| B. | t2时,反应已达到平衡状态 | |
| C. | t2-t3,各物质的浓度不再发生变化 | |
| D. | t2-t3,处于静止状态,反应不再发生 |
4.在密闭容器中进行X2(气)+2Y2(气)?Z(气)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
| A. | c(Z)=0.45mol/L | B. | c(Y2)=0.5mol/L | C. | c(X2)=0 | D. | c(X2)=0.5mol/L |
1.下列各组性质比较中,不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 碱性:KOH>NaOH>LiOH | ||
| C. | 单质的氧化性:F2<Cl2<Br2<I2 | D. | 单质的还原性:Al<Mg<Na |
18.下列哪种说法可以证明恒温恒容下,可逆反应.N2(g)+3H2(g)?2NH3(g)已达到平衡状态( )
| A. | 混合气体的密度不再改变 | |
| B. | 混合气体的平均分子量不再改变 | |
| C. | 混合气体中,N2、H2、NH3的物质的量之比为1:3:2 | |
| D. | 1个N≡N键断裂的同时,有6个N-H键形成 |
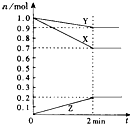 (1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:3X+Y
(1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:3X+Y 2Z
2Z