题目内容
8.0.8克O2中含3.01×1022个O,0.1克O2中含3.01×1022个质子.分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的构成计算.
解答 解:n(O)=$\frac{3.01×1{0}^{22}}{6.02×1{0}^{23}/mol}$=0.05mol,n(O2)=0.025mol,m(O2)=0.025mol×32g/mol=0.8g;
每个O原子含有8个质子,质子的个数为3.01×1022个,则物质的量为$\frac{3.01×1{0}^{22}}{6.02×1{0}^{23}/mol}$=0.05mol,n(O2)=$\frac{0.05mol}{16}$,m(O2)=$\frac{0.05mol}{16}$×32g/mol=0.1mol,
故答案为:0.8;0.1.
点评 本题考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握物质的构成以及相关公式的运用,难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
19.下列各组离子在溶液中既可以大量共存,且加氨水后不能产生沉淀的是( )
| A. | Na+ Ba2+ Cl- SO42- | B. | H+ NH4+ Al3+ SO42- | ||
| C. | H+ Cl- CH3COO- NO3- | D. | Na+ AlO2- NO3- OH- |
13.将10.4gNa20和Na2O2的固体混合物投入到水中.充分反应后收集到02的质量为 1.6g,则混合物中Na20的质量分数为( )
| A. | 20% | B. | 75% | C. | 25% | D. | 66% |
3.为了得到比较纯净的物质,使用的方法恰当的是( )
| A. | 向Na2CO3饱和溶液中,通入过量的CO2后,在减压、加热的条件下,蒸发得NaHCO3晶体 | |
| B. | 加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 向FeCl3溶液里加入足量NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3 |
20.从柑橘中可提炼得到结构为 的有机物,下列关于它的说法不正确的是( )
的有机物,下列关于它的说法不正确的是( )
 的有机物,下列关于它的说法不正确的是( )
的有机物,下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 其一氯代物有8种 | ||
| C. | 能与溴水发生加成反应 | D. | 难溶于水,且密度比水大 |
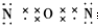 ,其空间构型是直线形,由此可知它是非极性(填“极性”或“非极性”)分子.
,其空间构型是直线形,由此可知它是非极性(填“极性”或“非极性”)分子.