题目内容
14.在0.1mol/L的CH3COOH溶液中,要促进醋酸电离,且c(H+)增大,应采取的措施是( )| A. | 加入0.1mol/L HCl | B. | 加入NaOH溶液 | ||
| C. | 升温 | D. | 加水 |
分析 醋酸为弱电解质,在溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加入的物质和醋酸根离子反应或升高温度才能使醋酸的电离平衡向右移动且c(H+)增大,据此分析解答.
解答 解:A.加入稀盐酸,溶液中氢离子浓度增大,抑制了醋酸的电离,导致醋酸的电离程度减小,故A错误;
B.加入氢氧化钠溶液,氢氧化钠和氢离子反应生成水,能促进醋酸的电离,但氢离子浓度减小,故B错误;
C.醋酸的电离是吸热反应,升高温度能促进醋酸的电离,且氢离子浓度增大,故C正确;
D.加水,促进了醋酸电离,但溶液中氢离子浓度减小,故D错误;
故选C.
点评 本题考查了影响弱电解质电离及其因素,题目难度不大,注掌握确弱电解质的电离平衡及其影响因素,明确本题中要求“要促进醋酸电离,且c(H+)增大”的含义,试题培养了学生灵活应用能力.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
4.下列化学式能代表其分子组成的是( )
| A. | SO2 | B. | SiO2 | C. | NH4Cl | D. | Mg |
2.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 60g丙醇中存在的共价键总数为10 NA | |
| B. | 1L 0.1mol/L NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA | |
| C. | 钠在空气中可生成多种氧化物.23g钠充分燃烧时转移电子数为1 NA | |
| D. | 235g核素${\;}_{92}^{235}$U发生裂变反应:${\;}_{92}^{235}$U+${\;}_{0}^{1}$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{34}^{136}$Xe+10${\;}_{0}^{1}$n,净产生的中子(${\;}_{0}^{1}$n)数为10 NA |
9.可以一次鉴别出乙酸、乙醇、乙酸乙酯三种物质的试剂是( )
| A. | 溴水 | B. | 饱和Na2CO3溶液 | C. | 石蕊试液 | D. | CuSO4溶液 |
8.咖啡鞣酸具有较广泛的抗菌作用,结构简式如图所示:关于咖啡鞣酸的下列叙述不正确的是( )
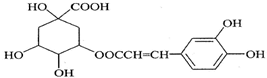
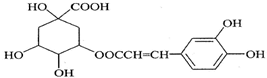
| A. | 分子式为C16H18O9 | |
| B. | 1 mol咖啡鞣酸水解时可消耗8molNaOH | |
| C. | 与苯环上碳直接相连的原子都在同一平面上 | |
| D. | 与浓溴水既能发生取代反应又能发生加成反应 |

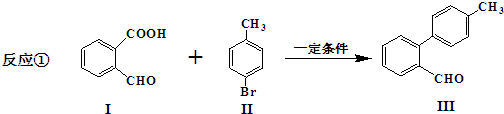
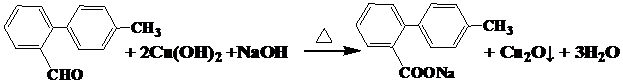 .
.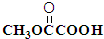 与
与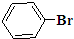 也可以发生类似反应①的反应,有机产物的结构简式为:
也可以发生类似反应①的反应,有机产物的结构简式为: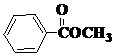 .
.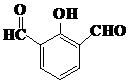 、
、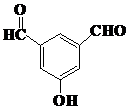 、
、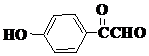 (任意两种).(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
(任意两种).(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)