题目内容
甲烷燃料电池,分别选择H2SO4溶液和NaOH溶液做电解质溶液,下列有关说法正确的是( )
| A、总反应方程式式都为CH4+2O2═CO2+2H2O |
| B、H2SO4和NaOH的物质的量都不变,但浓度都减小 |
| C、若用H2SO4溶液做电解质溶液,负极反应式为CH4-4e-+H2O═CO2+4H+ |
| D、若用NaOH溶液做电解质溶液,正极反应式为O2+2H2O+4e-═4OH- |
考点:化学电源新型电池
专题:电化学专题
分析:A、碱性条件下,二氧化碳与氢氧根离子反应生成碳酸根离子;
B、氢氧化钠参加反应;
C、负极上甲烷失电子;
D、正极上氧气得电子生成氢氧根离子.
B、氢氧化钠参加反应;
C、负极上甲烷失电子;
D、正极上氧气得电子生成氢氧根离子.
解答:
解:A、碱性条件下,二氧化碳与氢氧根离子反应生成碳酸根离子,则碱性条件下总反应方程式式都为2O2+CH4+2OH-═CO32-+3H2O,故A错误;
B、碱性条件下总反应方程式式都为2O2+CH4+2OH-═CO32-+3H2O,氢氧化钠参加反应,所以NaOH的物质的量减小,故B错误;
C、若用H2SO4溶液做电解质溶液,负极上甲烷失电子,负极反应式为CH4-8e-+2H2O═CO2+8H+,故C错误;
D、若用NaOH溶液做电解质溶液,正极上氧气得电子生成氢氧根离子,正极反应式为O2+2H2O+4e-═4OH-,故D正确;
故选D.
B、碱性条件下总反应方程式式都为2O2+CH4+2OH-═CO32-+3H2O,氢氧化钠参加反应,所以NaOH的物质的量减小,故B错误;
C、若用H2SO4溶液做电解质溶液,负极上甲烷失电子,负极反应式为CH4-8e-+2H2O═CO2+8H+,故C错误;
D、若用NaOH溶液做电解质溶液,正极上氧气得电子生成氢氧根离子,正极反应式为O2+2H2O+4e-═4OH-,故D正确;
故选D.
点评:本题考查原电池工作原理,题目难度中等,注意燃料电池中电极反应式的书写,应注意结合溶液的酸碱性书写电极反应式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
若锌与稀硝酸反应时,其化学反应方程式为4Zn+10HNO3═aZn(NO3)2+bM+cH2O,则a、b、c、M可能分别为( )
| A、4、1、5、N2O |
| B、4、2、4、NO2 |
| C、4、1、3、N2O4 |
| D、4、3、5、NO |
从原料和环境方面的要求看,绿色化学对生产中的化学反应提出一个提高原子利用率的要求,即尽可能不采用那些对产品的化学组成来说没有必要的原料.现有下列3种合成苯酚的反应路线:
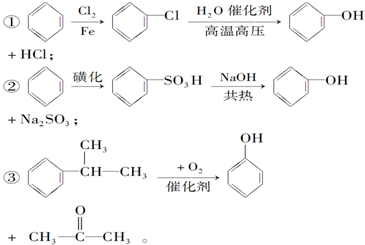
其中符合原子节约要求的生产过程是( )

其中符合原子节约要求的生产过程是( )
| A、③ | B、② | C、① | D、①②③ |
已知反应KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,据此判断下列说法正确的是( )
| A、反应物、生成物都属于电解质 |
| B、HCl全部发生氧化反应 |
| C、1mol KClO3在反应中得到6mol e- |
| D、该反应表明氧化性KClO3比Cl2强 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| D、常温常压下,18g H2O含有的中子数为10NA |
下列说法正确的是( )
A、按系统命名法,有机物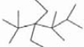 的命名为2,3,3,5,5一五甲基一4,4一二乙基己烷 的命名为2,3,3,5,5一五甲基一4,4一二乙基己烷 |
B、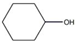 、 、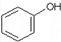 均能与碳酸钠溶液反应 均能与碳酸钠溶液反应 |
C、双酚 的一氯取代物有三种 的一氯取代物有三种 |
| D、工业采用分子筛固体酸作催化剂将苯和丙烯合成异丙苯,符合绿色化学工艺 |
下列说法正确的是( )
A、按系统命名法,化合物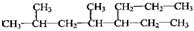 的名称为2,4-二甲基-5-丙基庚烷 的名称为2,4-二甲基-5-丙基庚烷 |
| B、人们生活中经常接触的聚乙烯、聚氯乙烯、聚苯乙烯、ABS工程塑料、顺丁橡胶等制品都是通过加聚反应得到的 |
| C、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| D、分子式为C4H8Br2的有机物,结构中只含一个甲基的同分异构体(不考虑立体异构)有5种 |
下列说法不正确的是( )
| A、在高温条件下,C能置换出SiO2中的Si,说明C的非金属性比Si强 |
| B、单质硅是将太阳能转化为电能的常用材料 |
| C、熔融烧碱不能使用石英坩埚和陶瓷坩埚 |
| D、置换反应一定是氧化还原反应,不一定是离子反应 |