题目内容
10.太空服以多种金属和胶黏剂作辅料,其中某种金属R可形成R2+.去掉其中可形成离子R2+的某种金属R形成阴离子Q2-,已知该离子的原子核内有n个中子,R原子的质量数为m.则W克该离子共含有的电子为( )| A. | $\frac{W(m-n)}{m}$mol | B. | $\frac{W(m-n+2)}{m}$mol | C. | $\frac{W(m-n-2)}{m}$mol | D. | $\frac{m-n-2}{Wm}$mol |
分析 太空服以多种金属和胶黏剂作辅料,其中某种金属R可形成R2+,去掉其中可形成离子R2+的某种金属R,形成的离子为带两个单位负电荷设为Q2-,根据质子数=质量数-中子数,阴离子:电子数=质子数+电荷数,以及n=$\frac{m}{M}$进行计算.
解答 解:太空服以多种金属和胶黏剂作辅料,其中某种金属R可形成R2+,去掉其中可形成离子R2+的某种金属R,形成的离子为带两个单位负电荷设为Q2-,Q2-离子的原子核内有n个中子,R原子的质量数为m,质子数=质量数-中子数=m-n,阴离子:电子数=质子数+电荷数=m-n+2,
故W克离子Q2-共含有的电子为$\frac{w(m-n+2)}{m}$mol,
故选B.
点评 本题考查利用原子构成的简单计算,明确质量数、质子数、中子数与电子数的关系是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
1.分子式为C5H10O2的有机物A,有果香味,在酸性条件下水解生成有机物B和C,其中C能被催化氧化成醛,则A可能的结构共有( )
| A. | 1种 | B. | 6种 | C. | 9种 | D. | 18种 |
18.SO2有毒,但葡萄酒里都含有SO2,起保鲜、杀菌和抗氧化作用.下列说法不正确的是( )
| A. | 葡萄酒中的SO2对人体无害,是因为它的含量很少 | |
| B. | 葡萄酒中的SO2具有抗氧化作用,是因为它具有较强的还原性 | |
| C. | 从红葡萄酒的颜色判断,其中的SO2没有漂白性 | |
| D. | 葡萄酒倒入酒杯摇一摇,可以减少其中SO2的含量 |
15.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
(1)在这些元素中,化学性质最不活泼的元素名称是氖,元素原子半径最小的是H,⑧号元素的离子结构示意图为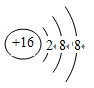 .
.
(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)⑧、⑨号元素的氢化物中还原性较强的是H2S(填化学式).
(4)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
(5)写出能说明⑨的非金属性比⑧强的一个实验事实氯气与硫化钠反应生成氯化钠和硫单质.
| 主族 周期 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
 .
.(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)⑧、⑨号元素的氢化物中还原性较强的是H2S(填化学式).
(4)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
(5)写出能说明⑨的非金属性比⑧强的一个实验事实氯气与硫化钠反应生成氯化钠和硫单质.
19.下列说法中错误的是( )
| A. | NH4H的电子式为: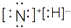 | B. | S2-的离子结构示意图为: | ||
| C. | H2O的形成过程: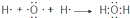 | D. | NaCl的形成过程: |
20.甲、乙、丙、丁四种物质分别含两种或三种元素,它们的分子中各含l8个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液只能与酸反应 | |
| B. | 丁和甲中各元素质量比相同,则丁中一定含有-l价的元素 | |
| C. | 丙中含有第二周期ⅣA族的元素,则丙一定是只含C、H的化合物 | |
| D. | 乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
 .
.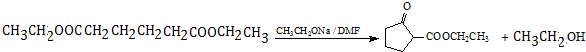 .
.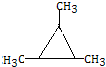 .
.