题目内容
对于复分解反应:X+Y→Z+W,下列叙述正确的是( )
| A、若Z是强酸,则X和Y必有一种是强酸 |
| B、若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
| C、若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
| D、若W是弱碱,Z是盐,则X和Y必有一种是强碱 |
考点:离子反应发生的条件
专题:离子反应专题
分析:A.有强酸生成的复分解反应中,反应物不一定有强酸,如H2S+CuSO4=CuS↓+H2SO4;
B.反应物为强酸和盐,则反应产物中可能生成强酸或弱酸;
C.反应物为强碱和盐,生成物中不一定有弱碱生成;
D.反应物中有一种碱性强于W即可,反应物中不一定为强碱.
B.反应物为强酸和盐,则反应产物中可能生成强酸或弱酸;
C.反应物为强碱和盐,生成物中不一定有弱碱生成;
D.反应物中有一种碱性强于W即可,反应物中不一定为强碱.
解答:
解:A.若Z是强酸,X和Y中可以都不是强酸,如:H2S+CuSO4=CuS↓+H2SO4,故A错误;
B.若X是强酸,Y是盐,反应后可以生成强酸,如浓硫酸与氯化钠反应生成氯化氢和硫酸钠,也可以是弱酸,如盐酸与碳酸钠生成碳酸:Na2CO3+2HCl=2NaCl+CO2↑+H2O,故B正确;
C.Y是强碱,X是盐,生成物Z和W可能都不是弱碱,如氢氧化钠与氯化铝的反应:AlCl3+4NaOH=NaAl(OH)4+3NaCl,反应生成两种盐,没有弱碱生成,故C错误;
D.若W是弱碱,Z是盐,则X和Y中不一定有强碱,如:氨水与氯化铝反应生成氢氧化铝和氯化铵:AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,一水合氨为弱碱,故D错误;
故选B.
B.若X是强酸,Y是盐,反应后可以生成强酸,如浓硫酸与氯化钠反应生成氯化氢和硫酸钠,也可以是弱酸,如盐酸与碳酸钠生成碳酸:Na2CO3+2HCl=2NaCl+CO2↑+H2O,故B正确;
C.Y是强碱,X是盐,生成物Z和W可能都不是弱碱,如氢氧化钠与氯化铝的反应:AlCl3+4NaOH=NaAl(OH)4+3NaCl,反应生成两种盐,没有弱碱生成,故C错误;
D.若W是弱碱,Z是盐,则X和Y中不一定有强碱,如:氨水与氯化铝反应生成氢氧化铝和氯化铵:AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,一水合氨为弱碱,故D错误;
故选B.
点评:本题考查了复分解反应的判断,题目难度不大,注意掌握复分解反应概念及反应原理,对各选项判断时找出反例即可,试题培养了学生的分析、理解能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某一溴代烷水解后的产物在红热铜丝催化下,最多可被空气氧化生成2种不同的醛,该一溴代烷的分子式可能是( )
| A、C3H7Br |
| B、C4H9Br |
| C、C5H11Br |
| D、C6H13Br |
下列有机物中,对于可能在一个平面上的最多原子数目的判断,正确的是( )
| A、丙烷最多有6个原子处于同一平面上 |
| B、环己烷最多有12个原子处于同一平面上 |
C、苯乙烯(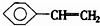 )最多有16个原子处于同一平面上 )最多有16个原子处于同一平面上 |
| D、CH3CH=CH-C≡C-CF3最多有10个原子处于同一平面上 |
下列对碱金属性质的叙述中,正确的是( )
| A、都是银白色的柔软金属,密度都比较小 |
| B、单质在空气中燃烧生成的都是过氧化物 |
| C、碱金属单质与水剧烈反应生成碱和氢气 |
| D、单质的熔、沸点随着原子序数的增加而升高 |
氯气是一种重要的工业原料.工业上利用反应在3Cl2+8NH3═N2+6NH4Cl检查氯气管道是否漏气.下列说法正确的是( )
| A、若管道漏气遇氨就会产生白雾 |
| B、该反应利用了氨气的还原性 |
| C、该反应属于复分解反应 |
| D、生成6mol NH4Cl有18mol电子转移 |
3个氨基酸(R-CH-COOH,烃基R可同可不同)失去2个H2O缩合成三肽化合物,现有分子式NH2为C36H57O18N11的十一肽化合物完全水解生成甘氨酸(C2H5O2N)、丙氨酸(C3H7O2N)、谷氨酸(C5H9O4N),在缩合成十一肽化合物时,这三种氨基酸的物质的量之比为( )
| A、3:3:5 |
| B、3:5:3 |
| C、5:3:3 |
| D、8:7:7 |
下列有关物质的性质及应用不正确的是( )
| A、氮气化学性质不活泼,所以可用于食品包装袋内防腐 |
| B、高铁酸钾(K2FeO4)具有强氧化性,经系列反应能产生某物质,能吸附水中杂质,故可用作自来水处理剂 |
| C、浓硫酸具有强氧化性,常温下使铁铝等金属钝化.故常温下可用铁制容器运输浓硫酸 |
| D、二氧化硫有漂白作用,在KMnO4溶液中通入二氧化硫,可起到漂白作用 |
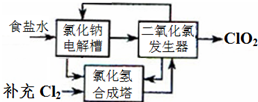 二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.
二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.