题目内容
12.设阿伏加德罗常数为NA,下列说法正确的是( )| A. | 标准状况下,22.4L乙烷含共价键数目为7NA | |
| B. | 25℃时,1.0LpH=13的Ba(OH)2溶液含OH-数目为0.2NA | |
| C. | 铝与氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA | |
| D. | 常温常压下,6gHe含中子数为2NA |
分析 A、根据n=$\frac{V}{{V}_{m}}$计算乙烷的物质的量,每个乙烷分子含有7个共价键,再根据N=nNA计算共价键数目;
B、根据pH值计算氢离子浓度,再根据Kw计算氢氧根的浓度,利用n=cV计算氢氧根的物质的量,根据N=nNA计算氢氧根离子数目;
C、铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,氢元素化合价由+1价降低为0价,根据氢气计算电子转移;
D、根据n=$\frac{m}{M}$计算4He的物质的量,4He中子数为2,再根据N=nNA计算中子数目.
解答 解:A、标准状况下,22.4L乙烷含共价键数目为$\frac{22.4L}{22.4L/mol}$×7×NAmol-1=7NA,故A正确.
B、pH=13的Ba(OH)2溶液,c(OH-)=0.1mol/L,所以1.0LpH=13的Ba(OH)2溶液含OH-数目为1.0L×0.1mol/L×NAmol-1=0.1NA,故B错误;
C、铝与氢氧化钠溶液反应生成1mol氢气时,转移的电子数为1mol×2×NAmol-1=2NA,故C错误;
D、4He中子数为2,6g4He含中子数为$\frac{6g}{4g/mol}$×2×NAmol-1=3NA,故D错误;
故选:A.
点评 本题考查阿伏伽德罗常数分析应用,主要是常用化学计量数的有关计算,难度不大,注意公式的运用.

练习册系列答案
相关题目
2.某同学在实验报告中有以下的实验数据:
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
| A. | ①②③ | B. | ①③④ | C. | ①②③④ | D. | ①④ |
3.下列的判断或说法不正确的是( )
| A. | 溶解少量食盐于水中:△S>0 | |
| B. | 自发一定是放热反应 | |
| C. | 自发反应一定是熵增加或者放热反应 | |
| D. | CaCO3 (S) 分解成CaO (S) 和 CO2(g):△S>0 |
20.下列物质中,不属于电解质的是( )
| A. | 乙醇 | B. | CH3COOH | C. | BaCl2 | D. | Cl2 |
17.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关.当n(KOH)=a mol时,下列有关说法错误的是( )
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{{O}_{3}}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量等于$\frac{1}{2}$a mol | |
| C. | 改变温度,产物中KClO的最大理论产量为$\frac{1}{2}$a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$a mol |
4.有机物分子中基团之间的相互影响会导致物质化学性质的不同.下列事实能说明上述观点的是 ( )
| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 苯在50℃~60℃时发生硝化反应,而甲苯在30℃时即可 |
1.下列解释事实的方程式不准确的是( )
| A. | 铝热法炼铁:Fe2O3+2Al$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+2Fe | |
| B. | 工业上用NH3制备NO:4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O | |
| C. | 向受酸雨影响的湖泊中喷洒CaCO3粉末:CO32-+2H+$\frac{\underline{\;催化剂\;}}{\;}$H2O+CO2↑ | |
| D. | 过氧化钠用于呼吸面具中作为氧气的2Na2O2+2CO2═2Na2CO3+O2 |
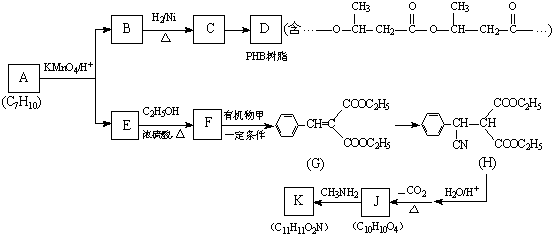
 $\stackrel{KMnO4/H+}{→}$RCOOH+
$\stackrel{KMnO4/H+}{→}$RCOOH+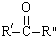
 +H2O
+H2O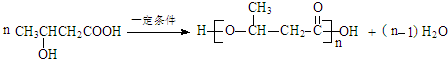 .
.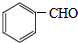 .
. .
.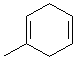 .
.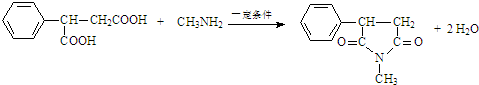 .
.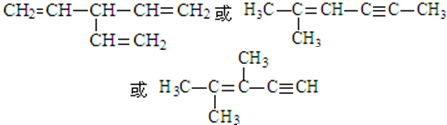 (写出一种即可).
(写出一种即可).