题目内容
19.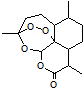 2015年,中国药学家屠呦呦获得诺贝尔生理学或医学奖,其突出贡献是创制新型抗疟药青蒿素和双氢青蒿素.已知青蒿素的结构如图所示,有关青蒿素的说法,不正确的是( )
2015年,中国药学家屠呦呦获得诺贝尔生理学或医学奖,其突出贡献是创制新型抗疟药青蒿素和双氢青蒿素.已知青蒿素的结构如图所示,有关青蒿素的说法,不正确的是( )| A. | 分子式为C15H22O5 | |
| B. | 能够发生水解反应 | |
| C. | 每个分子中含有4个六元环 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键基团有关 |
分析 可根据有机物的结构简式判断分子式为C15H22O5,分子中含有-O-O-键,具有强氧化性,含有-COO-,可发生水解反应,以此解答.
解答 解:A.根据有机物的结构简式判断分子式为C15H22O5,故A正确;
B.含有酯基,可发生水解反应,故B正确;
C.由结构可知,含有3个六元环 2个七元环,故C错误;
D.分子中含有过氧键,具有较强的氧化性,可用于杀菌消毒,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,题目难度中等,注意把握有机物官能团的结构和性质.

练习册系列答案
相关题目
9.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | c(H+)=1×10-1 mol•L-1的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| D. | 0.1mol•L-1CH3COONa溶液:H+、Al3+、Cl-、NO3- |
14.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )
| A. |  称量药品 | B. | 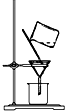 过滤 | C. | 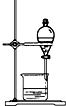 分离乙醇和水 | D. | 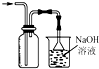 收集氯气 |
4.25℃时,用0.1mol•L-1的CH3COOH溶液滴定20mL0.1mol•L-1的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7.已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是( )
| A. | Ka=$\frac{2×1{0}^{-7}}{0.1V-2}$ | B. | V=$\frac{2×1{0}^{-7}}{0.1Ka-2}$ | ||
| C. | K a=$\frac{2×1{0}^{-7}}{V+20}$ | D. | K a=$\frac{2×1{0}^{-8}}{V}$ |
11.已知,H2和I2反应的历程为:①I2+M?2I•+M慢 ②H2+2I•→2HI快式中M是指反应器壁或其他惰性分子,不参与反应,只具有传递能量的作用.下列关于该反应的说法正确的是( )
| A. | 反应速率与I•的浓度有关 | B. | M是该反应的催化剂 | ||
| C. | 反应①与②的活化能相等 | D. | v(H2)=v(I2)=v(HI) |
8.下表数据是对应物质的熔点,下列说法错误的是( )
| 编号 | ① | ② | ③ | ④ |
| 物质 | AlF3 | AlCl3 | BCl3 | NCl3 |
| 熔点/℃ | 1291 | 160 | -107 | -40 |
| A. | BCl3、NCl3分子中各原子最外层都满足8电子稳定结构 | |
| B. | NCl3中心原子价层电子对数比BCl3中心原子价层电子对数多 | |
| C. | AlF3、AlCl3都是强电解质,但晶体类型不同 | |
| D. | BCl3为平面正三角形分子,故它是由极性键构成的非极性分子 |
 ;
; ;指出分子中化学键是共价键(填‘离子键’或‘共价键’).
;指出分子中化学键是共价键(填‘离子键’或‘共价键’).