题目内容
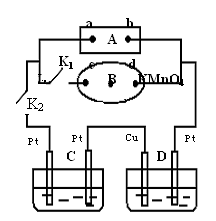
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是
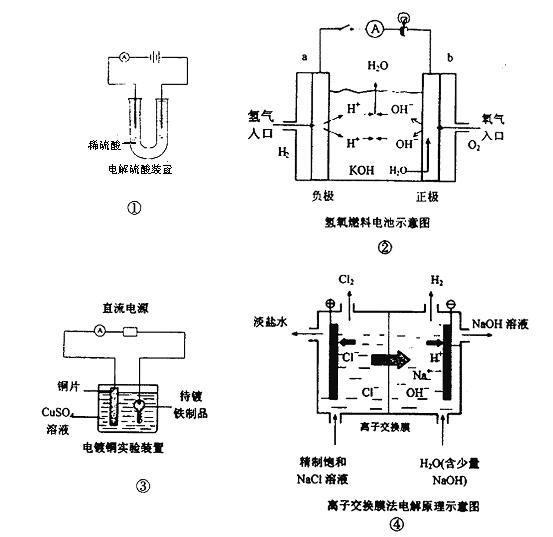

| A.装置①中电解一段时间后,溶液的PH不变。 |
| B.装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O |
| C.装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol 电子转移,此时铜片和铁制品的质量差为128g |
| D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
C
A项,电解稀硫酸实质是电解水,电解过程中,硫酸的物质的量不变,溶液的体积减少,H+的浓度增大,溶液的PH减少;B项,该电池的电解质溶液为KOH溶液,故该极的电极反应式应为O2+2H2O+4e-=4OH-;C项,阴极反应式:Cu2++2e-="Cu" ,即2mol电子转移时铜片质量增加64克,阳极反应式:Cu-2e-= Cu2+,当2mol电子转移时,铜片质量减少64克,故铜片和铁制品的质量差为128g。D项,阳离子交换膜上每透过1mol Na+时,电子转移1mol,据阴极反应式:2H+ + 2e-+ =H2 ↑,若在标准状况下,产生11.2L H2,但题意中无此条件,故D项错。

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
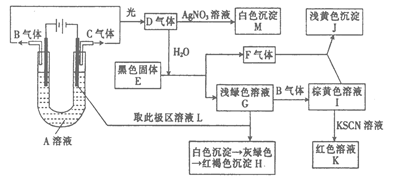
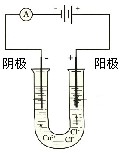
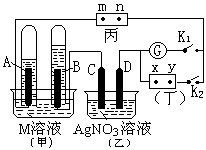
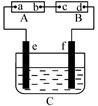
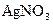 溶液中,通电电解,当电解液的pH从6.0变为3.0时(电解质溶液电解前后体积的变化忽略不计),则电极上应析出的银的质量是
溶液中,通电电解,当电解液的pH从6.0变为3.0时(电解质溶液电解前后体积的变化忽略不计),则电极上应析出的银的质量是