题目内容
【题目】下列实验过程可以达到实验目的的是
编号 | 实验目的 | 实验过程 |
A | 配制0.4000 mol·L1的NaOH溶液 | 称取4.0 g固体NaOH于250 mL容量瓶中,加入蒸馏水溶解,定容至刻度线即可。 |
B | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
C | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
D | 制备Fe(OH)3胶体 | 通常是将Fe(OH)3固体溶于热水中即可 |
A. A B. B C. C D. D
【答案】B
【解析】
A. 不能在容量瓶中溶解物质,称取固体质量“4.0g”不能满足配制溶液的浓度“0.4000mol/L”的精确度,A项错误;
B.氯化铁具有较强的氧化性,若被还原剂还原则生成FeCl2,溶液颜色由棕黄色变成浅绿色,所以向氯化铁溶液中加浓的维生素C溶液,如果有颜色变化,即可证明维生素C有还原性,B项正确;
C.MgCl2属于强酸弱碱盐,发生水解反应:MgCl2+2H2O![]() Mg(OH)2+2HCl,生成的HCl具有挥发性,加热MgCl2溶液过程中水解产生的HCl随水蒸气挥发,溶液中HCl浓度逐渐减小,水解平衡向正反应方向移动,最终水解完全,蒸干得到Mg(OH)2,所以将MgCl2溶液蒸干,不能得到无水MgCl2,C项错误;
Mg(OH)2+2HCl,生成的HCl具有挥发性,加热MgCl2溶液过程中水解产生的HCl随水蒸气挥发,溶液中HCl浓度逐渐减小,水解平衡向正反应方向移动,最终水解完全,蒸干得到Mg(OH)2,所以将MgCl2溶液蒸干,不能得到无水MgCl2,C项错误;
D.Fe(OH)3固体颗粒较大又难溶于水,直接将Fe(OH)3放入热水中,无法在水中形成粒子直径在1nm~100nm之间的Fe(OH)3固体颗粒,不能得到Fe(OH)3胶体,D项错误;答案选B。

 考前必练系列答案
考前必练系列答案【题目】温度为T1时,将气体X和气体Y各1.6mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 1.2 | 1.1 | 1.0 | 1.0 |
A. 反应0~4 min的平均速率υ(Z)=0.25 mol/(Lmin)
B. T1时,反应的平衡常数K1=1.2
C. 其他条件不变,9 min后,向容器中再充入1.6 molX,平衡向正反应方向移动,再次达到平衡时X的浓度减小,Y的转化率增大
D. 其他条件不变,降温到T2达到平衡时,平衡常数K2=4,则此反应的△H<0
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺流程如下:

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe2+、Al3+、Ca2+和Mg2+。②Cr2O72-+H2O![]() 2CrO42-+2H+。③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
2CrO42-+2H+。③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe2+ | Mg2+ | Al3+ | Cr3+ |
沉淀完全时的pH | 3.2 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1) 实验室用18.4mol/L的浓硫酸配制480mL2mol/L的硫酸,需量取浓硫酸_____mL;配制时除量筒、烧杯和玻璃棒外,还需用到的玻璃仪器有______________。
(2) H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:__________。
(3过滤II操作得到的滤渣主要为______(填化学式),滤液II中含有的离子主要有__。
(4) 钠离子交换树脂的反应原理为:Mn++nNaR=MRn+nNa+,则利用钠离子交换树脂可除去滤液II中的金属阳离子有_______________。
(5) 写出上述流程中用SO2进行还原时发生反应的离子方程式__________。
【题目】下列有关实验的选项正确的是
|
|
|
|
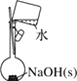
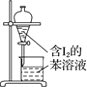
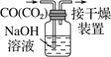
A.配制 0.10 mol·L-1NaOH溶液 | B.苯萃取碘水中I2,分出水层后的操作 | C.除去CO中的CO2 | D.记录滴定终点读数为12.20mL |
A. A B. B C. C D. D