题目内容
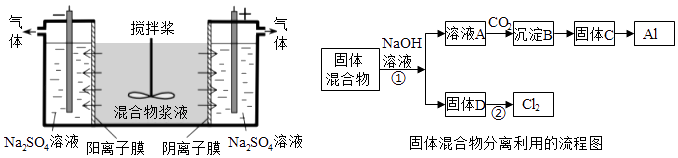
【题目】下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法不正确的是( )
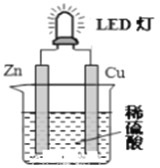
A. 铜片表面有气泡生成,且溶液中SO42-向该电极移动
B. 装置中存在“化学能→ 电能→ 光能”的转换
C. 如果将硫酸换成柠檬汁,导线中仍有电子流动
D. 如果将锌片换成铁片,电路中的电流方向不变
【答案】A
【解析】A.铜锌原电池中,Cu作正极,溶液中的氢离子在正极上得电子生成氢气,所以Cu上有气泡生成,溶液中的阴离子向负极移动,故A错误;B.原电池中化学能转化为电能,LED灯发光时,电能转化为光能,故B正确;C.柠檬汁显酸性也能作电解质溶液,所以将硫酸换成柠檬汁,仍然构成原电池,所以导线中有电子流动,故C正确;D.金属性Cu比Zn、Fe弱,Cu作正极,所以电路中的电流方向不变,仍然由Cu流向负极,故D正确;故选A。

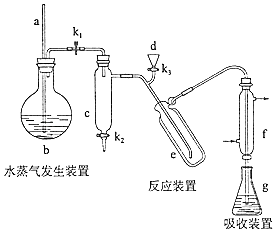
【题目】已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )

选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>I2 Cl2>Br2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Cl->Fe2+ |
A. A B. B C. C D. D
【题目】I.一定量的CO(g)和H2O(g)分别通入容积为1L的恒容密闭容器中,发生反应CO(g)+H2OCO2(g)+H2(g)得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衝所需时间/min | |
CO | H2O | CO2 | |||
1 | 500 | 8 | 4 | 3.2 | 4 |
2 | 700 | 4 | 2 | 0.8 | 3 |
3 | 700 | 4 | 2 | 0.8 | 1 |
(1)①下列情况表明反应达到平衡状态的是 (填序号)
A.CO2和H2生成速率相等
B.温度不变时,压强不变
C.生成CO2的速率和生成CO的速率相等
②实验2中,反应达到平衡状态时,CO的转化率为 .
③实验3和实验2相比,改变的条件是 .
(2)①硫化钠溶液具有较强碱性,其原因是(用离子方程式表示).
②欲使0.1mol的Na2S溶液中, ![]() 的值增大,可采取的措施是(填序号)
的值增大,可采取的措施是(填序号)
A.加适量等浓度的NaOH溶液
B.加适量的水
C.通入适量的H2S气体.