题目内容
【题目】(1)相同物质的量的O2和O3的质量比______,分子个数比为_______,所含氧原子的个数比为_______。
(2)在200 mL 2 mol·L-1MgCl2溶液中,溶质的质量为_______。Cl-的物质的量浓度为__________。
【答案】2:3 1:1 2:3 38g 4mol/L
【解析】
(1)依据n=![]() =
=![]() ,结合臭氧三原子分子、氧气双原子分子解答;
,结合臭氧三原子分子、氧气双原子分子解答;
(2)依据n=cV,m=nM,结合氯化镁为强电解质,完全电离,1mol氯化镁含有2mol氯离子解答。
(1)依据n=![]() =
=![]() 可知,物质的量相等,物质的质量与摩尔质量成正比;分子数与物质的量成正比,所以相同物质的量的O2和O3的质量比为32:48=2:3;分子数之比为1:1;臭氧三原子分子、氧气双原子分子,所以相同物质的量的O2和O3的所含氧原子的个数比为:1×2:1×3=2:3;故答案为:2:3;1:1;2:3;
可知,物质的量相等,物质的质量与摩尔质量成正比;分子数与物质的量成正比,所以相同物质的量的O2和O3的质量比为32:48=2:3;分子数之比为1:1;臭氧三原子分子、氧气双原子分子,所以相同物质的量的O2和O3的所含氧原子的个数比为:1×2:1×3=2:3;故答案为:2:3;1:1;2:3;
(2)在200mL 2mol/L MgCl2溶液中,溶质的质量为:2mol/L×0.2L×95g/mol=38g;氯化镁为强电解质,完全电离,1mol氯化镁含有2mol氯离子,氯化镁溶液中氯离子物质量浓度等于氯化镁物质的量浓度2倍,为4 mol/L;故答案为:38g;4mol/L。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
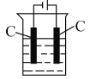
活力试卷系列答案【题目】某研究性学习小组同学为了探究“在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子”,他们以教材中相关(科学探究)为基础,设计了如图实验装置并记录相关实验数据。
(实验装置)
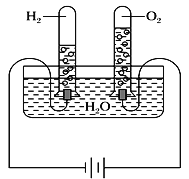
(部分实验数据)
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30 ℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30 ℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2的物质的量分别是________mol、________mol。
(2)该温度下,气体摩尔体积是__________。
(3)在该实验条件下,3 mol O2的气体的体积为____________L