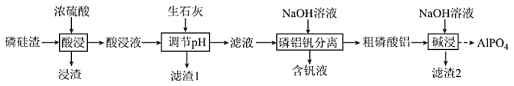
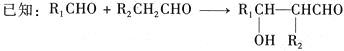题目内容
【题目】有机化合物M是一种药品辅料的中间体,下图是该有机化合物的合成线路。请回答下列问题。
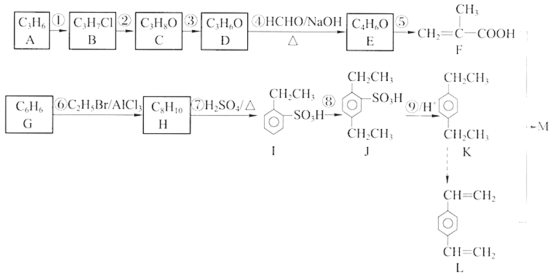
已知: i.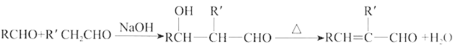
ii.两种或两种以上的单体发生的加聚反应称为共聚反应,如:

(1)A的结构简式是_________。
(2)反应②的化学方程式是_________。
(3)合成线路①~⑤中属于氧化反应的有_________(填序号)。
(4)反应④的化学方程式是_________。
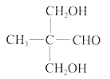
(5)若1mol D与2mol HCHO反应,该反应产物的结构简式是_________。
(6)反应⑧的反应物及反应条件是_________。
(7)合成线路中⑦~⑨的目的是_________。
(8)在一定条件下,F与L按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是_________。
【答案】CH3CH=CH2 CH3CH2CH2Cl+NaOH![]() CH3CH2CH2OH+NaCl ③⑤
CH3CH2CH2OH+NaCl ③⑤ 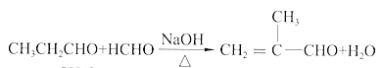
 反应物是C2H5Br, 用AlCl3作催化剂 利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生
反应物是C2H5Br, 用AlCl3作催化剂 利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生 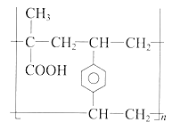
【解析】
结合E的分子式和F的结构简式可知,E氧化生成F,推知E为![]() ,D与甲醛在氢氧化钠中加热发生类似已知: i.
,D与甲醛在氢氧化钠中加热发生类似已知: i.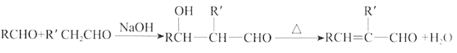 的反应,得到E,可推知D为CH3CH2CHO,C为CH3CH2CH2OH,B为CH3CH2CH2Cl,则A为CH3CH=CH2;苯与溴乙烷在氯化铝作用下发生反应生成乙苯H,乙苯与浓硫酸发生磺化反应生成I为邻乙基苯磺酸,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J为
的反应,得到E,可推知D为CH3CH2CHO,C为CH3CH2CH2OH,B为CH3CH2CH2Cl,则A为CH3CH=CH2;苯与溴乙烷在氯化铝作用下发生反应生成乙苯H,乙苯与浓硫酸发生磺化反应生成I为邻乙基苯磺酸,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J为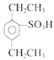 ,
, 酸化得到K为
酸化得到K为![]() ,
,![]() 在一定条件下发生一系列反应得到L为
在一定条件下发生一系列反应得到L为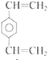 ,
, 与
与![]() 反应生成M为
反应生成M为 ,据此分析解答。
,据此分析解答。
(1)根据以上分析,A的结构简式是CH3CH=CH2;
(2)反应②是CH3CH2CH2Cl在氢氧化钠的水溶液中加热发生水解反应生成CH3CH2CH2OH和氯化钠,反应的化学方程式是CH3CH2CH2Cl+NaOH![]() CH3CH2CH2OH+NaCl;
CH3CH2CH2OH+NaCl;
(3)合成线路①~⑤中属于氧化反应的有③⑤;
(4)反应④是丙醛和甲醛在氢氧化钠中加热发生反应生成![]() 和水,反应的化学方程式是
和水,反应的化学方程式是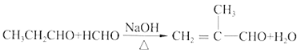 ;
;
(5)若1mol D(CH3CH2CHO)与2mol HCHO反应,丙醛中醛基相连的碳上两个碳氢键断裂加成在甲醛上,该反应产物的结构简式是 ;
;
(6)反应⑧与反应⑥相似,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J,反应物是C2H5Br,用AlCl3作催化剂;
(7)合成线路中⑦~⑨的目的是利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生;
(8)在一定条件下,F(![]() )与L(
)与L( )按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是
)按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是 。
。

 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
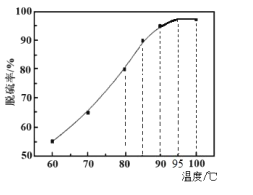
快乐5加2金卷系列答案【题目】丙烯酸酯类物质广泛用于建筑、包装材料等,丙烯酸是合成丙烯酸酯的原料之一。丙烯醇可用于生产甘油、塑料等。以丙烯醛为原料生产丙烯醇、丙烯酸的流程如图所示:
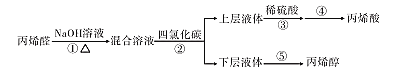
已知:
①2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
②2CH2=CHOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有关物质的相关性质如表:
物质 | 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
沸点/℃ | 53 | 97 | 141 | 77 |
熔点/℃ | - 87 | - 129 | 13 | -22.8 |
密度/g·mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
溶解性(常温) | 易溶于水和有机溶剂 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 难溶于水 |
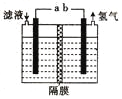
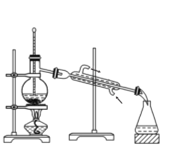
(1)操作①需要连续加热30min,所用装置如图所示。仪器L名称是________。
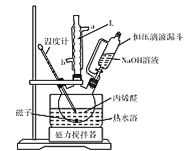
(2)操作②使用的主要仪器是分液漏斗,在使用之前需进行的操作是 ___。
(3)操作④包括____、过滤、冰水洗涤、低温吸干。
(4)操作⑤中,加热蒸馏“下层液体”,分离出四氯化碳;再分离出丙烯醇(如图),要得到丙烯醇应收集 ____(填温度)的馏分。图中有一处明显错误,应改为____。
(5)测定丙烯醇的摩尔质量:准确量取amL丙烯醇于分液漏斗中,烧瓶内盛装足量钠粒。实验前量气管B中读数为b mL,当丙烯醇完全反应后,冷却至室温、调平B、C液面,量气管B的读数为c mL。已知室温下气体摩尔体积为VL·mol-1。
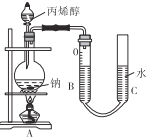
调平B、C液面的操作是____;实验测得丙烯醇的摩尔质量为____g·mol-1(用代数式表示)。如果读数时C管液面高于B管,测得结果将____(填“偏大”“偏小”或“不变”)。
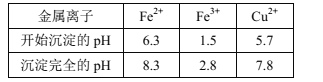
【题目】氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.2000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1) 配平离子方程式:______MnO4-+HSO3-+H+=Mn2++SO42-+H2O。
(2)用KMnO4进行滴定时,KMnO4溶液应装在_______________中,判断滴定终点的现象是_______。
(3)下列操作会导致测定结果偏高的是_________。
A. 盛装未知浓液的锥形瓶用蒸馏水洗过,未用待测液润洗
B. 未用标准浓度的酸性KMnO4溶液润洗滴定管
C. 观察读数时,滴定前仰视,滴定后俯视
D. 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
(4) 根据下表测定的实验数据,计算KMnO4溶液体积的平均值为___mL;NaHSO3溶液的物质的量浓度为___mol/L(数据精确到0.1)。
试验编号 | 待测NaHSO3溶液的体积/ mL | KMnO4溶液体积/ mL |
1 | 20.00 | 15.98 |
2 | 20.00 | 17.00 |
3 | 20.00 | 16.02 |