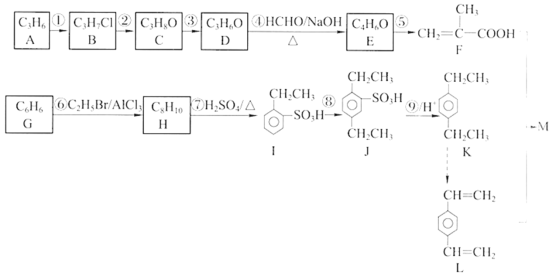
题目内容
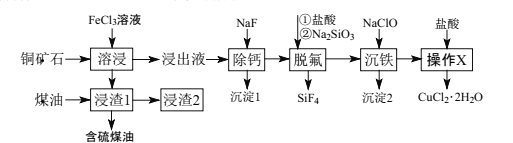
【题目】辉铜矿石主要含有硫化亚铜(Cu2S),还含有FeO、CaO、SiO2等。以辉铜矿石为原料制备CuCl2·2H2O的工艺流程如图所示:
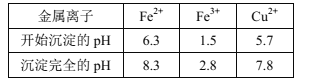
已知:Ⅰ.金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
Ⅱ.NaCl易溶于水,不溶于酒精,随温度变化溶解度变化不明显;CuCl2·H2O易溶于水,酒精,浓氨水,随温度升高溶解度变化明显增大。
Ⅲ.Ksp(CaF2)=4.0×10-11
(1)为了提高“溶浸”效率,可采取的措施是___。写出“溶浸”过程中Cu2S溶解时离子方程式:___。
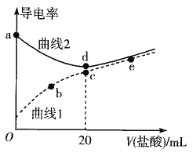
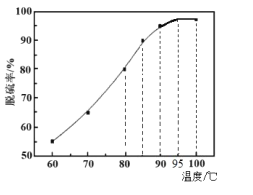
(2)“脱硫”时,随着温度的升高,脱硫率呈上升趋势(如图),原因是___。
(3)写出“脱氟”时HF发生反应的化学方程式:___。
(4)“沉铁”过程中,加入NaClO的两个作用是___。
(5)“操作X”的具体操作是___。
(6)经过“操作X”后,母液经过一系列操作可得到另外一种物质,要得到这种纯净物,最好选用下列试剂洗涤___。
A.浓盐酸 B.水 C.酒精 D.浓氨水
(7)向“浸出液”中加入NaF除去溶液中Ca2+(浓度为1.0×10-3mol·L-1),当溶液中c(F-)=2.0×10-3mol·L-1时,除钙率为___。
【答案】将矿石细磨(搅拌、升温或其它合理答案) Cu2S+4Fe3+=S+4Fe2++2Cu2+ 温度升高,单质硫在煤油中的溶解度增加 4HF+H2SiO3=SiF4↑+3H2O NaClO将Fe2+氧化Fe3+,消耗H+,使H+浓度减小,促使水解平衡Fe3++3H2O![]() Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀 蒸发浓缩 冷却结晶 C 99%
Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀 蒸发浓缩 冷却结晶 C 99%
【解析】
辉铜矿加入氯化铁溶液溶解浸取过滤,得到矿渣加入煤油回收硫单质;加入NaF除去钙离子,生成CaF2沉淀,加盐酸和硅酸钠生成H2SiO3除去多余的氟离子,再用NaClO将Fe2+氧化Fe3+,消耗H+,使H+浓度减小,促使水解平衡Fe3++3H2O![]() Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;过滤后在滤液中加入盐酸调节pH,蒸发浓缩 冷却结晶,得到CuCl2·H2O。
Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;过滤后在滤液中加入盐酸调节pH,蒸发浓缩 冷却结晶,得到CuCl2·H2O。
(1)为了提高“溶浸”效率,可采取的措施是将矿石细磨(搅拌、升温或其它合理答案);“溶浸”过程中Cu2S溶解时,被Fe3+氧化,离子方程式:Cu2S+4Fe3+=S+4Fe2++2Cu2+。
故答案为:将矿石细磨(搅拌、升温或其它合理答案);Cu2S+4Fe3+=S+4Fe2++2Cu2+;
(2)“脱硫”时,随着温度的升高,脱硫率呈上升趋势,温度升高,单质硫在煤油中的溶解度增加;
故答案为:温度升高,单质硫在煤油中的溶解度增加;
(3)加盐酸和硅酸钠生成H2SiO3除去多余的氟离子,“脱氟”时HF发生反应的化学方程式:4HF+H2SiO3=SiF4↑+3H2O。
故答案为:4HF+H2SiO3=SiF4↑+3H2O;
(4)“沉铁”过程中,加入NaClO的两个作用是NaClO将Fe2+氧化Fe3+,消耗H+,使H+浓度减小,促使水解平衡Fe3++3H2O![]() Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;
Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;
故答案为:NaClO将Fe2+氧化Fe3+,消耗H+,使H+浓度减小,促使水解平衡Fe3++3H2O![]() Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;
Fe(OH)3+3H+向右移动,生成Fe(OH)3沉淀;
(5)氯化铜溶于水,则“操作X”的具体操作是蒸发浓缩 冷却结晶。
故答案为:蒸发浓缩 冷却结晶
(6)经过“操作X”后,母液经过一系列操作可得到另外一种物质,这种物质是NaCl,NaCl易溶于水,不溶于酒精,随温度变化溶解度变化不明显;CuCl2·H2O易溶于水、酒精、浓氨水,随温度升高溶解度变明显增大。所以要得到这种纯净物,最好选用洗涤剂酒精,而A.浓盐酸、B.水、D.浓氨水三个选项中提供的物质均能溶解NaCl,故答案为:C。
(7)当溶液中c(F-)=2.0×10-3mol·L-1时,Ksp(CaF2)=c(Ca2+)c2(F-)=c(Ca2+)(2.0×10-3)2= 4.0×10-11,c(Ca2+)=1.0×10-5mol·L-1,则除钙率为![]() ×100%=99%。
×100%=99%。
故答案为:99%。

【题目】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。
Ⅰ.经查:①Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10;②Ka(HNO2)=5.1×10-4。请设计最简单的方法鉴别NaNO2和NaCl两种固体______________________
Ⅱ. 某小组同学用如下装置(略去夹持仪器)制备亚硝酸钠
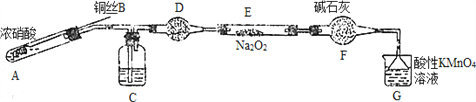
已知:①2NO+Na2O2=2NaNO2; ②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+。
(1)使用铜丝的优点是________________________。
(2)装置A中发生反应的化学方程式为_____________________________。
装置C中盛放的药品是_________;(填字母代号)
A.浓硫酸 B.NaOH溶液 C.水 D.四氯化碳
(3)该小组称取5.000g制取的样品溶于水配成250ml溶液,取25.00ml溶液于锥形瓶中,
用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是_________(填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________。
③该样品中亚硝酸钠的质量分数为______________。