题目内容
【题目】(题文)某兴趣小组设计了如图所示装置(部分夹持装置已略去)进行实验探究。
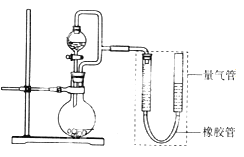
(实验一)探究影响化学反应速率的因素。
圆底烧瓶中装锌片(两次实验中所用锌片大小和外形相同)、恒压分液漏斗中装稀硫酸,以生成20.0mL气体为计时终点,结果为t1>t2。
序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s | ||||
I | 40 | 1 | t1 | ||||
II | 40 | 3 | t2 | ||||
序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s | ||||
I | 40 | 1 | t1 | ||||
II | 40 | 3 | t2 | ||||
检查该装置气密性的方法是_______________________________________________。
比较实验I和Ⅱ可以得出的结论是____________________________________________。
(实验二)探究铁的电化学腐蚀。
①圆底烧瓶中装铁粉和碳粉混合物,恒压分液漏斗中装稀硫酸,打开活塞加入稀硫酸后量气管中出现的现象是:左侧液面_________右侧液面_________(选填“上升”、“下降”)。
②圆底烧瓶中装与①相同量的铁粉但不加入碳粉,其他试剂和操作相同,发现左、右侧液面变化较_______(选填“快”、“慢”,下同),说明原电池反应比一般化学反应_______。
③圆底烧瓶中装与①相同量的铁粉和碳粉混合物,恒压分液漏斗中装食盐水,打开活塞加入食盐水后,你预测量气管中出现的现象是:___________________________________,正极的电极反应是___________________________。
【答案】从量气管右侧管口加水至左右两管出现液面高度差时停止加水,若能保持液面高度差不变,则说明装置气密性好 增大反应物浓度能加快化学反应速率下降上升慢快左侧液面上升右侧液面下降O2 + 4e- + 2H2O = 4OH-
【解析】
本题考查了化学反应的速率的影响因素,钢铁的电化学腐蚀等,注意知识的归纳和梳理是关键。
【实验一】由实验装置分析得检验气密性的方法是从量气管右侧管口加水至左右两管出现液面高度差时停止加水,若较长时间能保持液面高度差不变,则说明装置气密性好; t1>t2,说明实验Ⅱ反应速率较大,二者浓度不同,说明在气体条件一定时,反应收益率随着反应物浓度的增大而增大;【实验二】①铁和硫酸反应生成硫酸亚铁和氢气,有气体生成,而且放热,所以压强增大,所以左侧液面下降,右侧液面上升;②圆底烧瓶中装与①相同量的铁粉但不加入碳粉,其他试剂和操作相同,因为①中形成的原电池 ,反应快,所以不加碳粉的反应慢;③圆底烧瓶中装与①相同量的铁粉和碳粉混合物,恒压分液漏斗中装食盐水,打开活塞加入食盐水后,铁发生吸氧腐蚀,左侧空气量减少,左侧液面上升,右侧液面下降;空气中的氧气在正极得到电子发生反应,电极反应为: O2 + 4e- + 2H2O = 4OH-。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
