题目内容
15.NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.
(1)上述反应中氧化剂是NaNO2.
(2)根据上述反应,鉴别NaNO2和NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有①②⑤(填序号).
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是B(填编号).
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式:
10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mol e-,则生成标准状况下N2的体积为11.2L.
(5)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图:
①第一步反应是放热反应(填“放热”或“吸热”),判断依据是反应物总能量大于生成物总能量.
②1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol.
分析 (1)反应中N元素的化合价降低,I元素的化合价升高;
(2)由2NaNO2+4HI═2NO↑+I2+2NaI+2H2O可知,鉴别NaNO2和NaCl,可利用碘的特性分析;
(3)NaNO2具有氧化性,能使NaNO2转化为不引起二次污染的N2的物质应具有还原性;
(4)Al元素的化合价由0升高为+3价,N元素的化合价由+5价降低为0,由电子守恒及原子守恒分析;
(5)①第一步反应中,反应物总能量大于生成物总能量;
②1mol NH4+(aq)全部氧化成NO3-(aq)可由两步反应加和得到.
解答 解:(1)反应中N元素的化合价降低,I元素的化合价升高,则氧化剂是NaNO2,故答案为:NaNO2;
(2)由2NaNO2+4HI═2NO↑+I2+2NaI+2H2O可知,鉴别NaNO2和NaCl,则选择①水②碘化钾淀粉试纸⑤食醋,变蓝的为NaNO2,故答案为:①②⑤;
(3)NaNO2具有氧化性,能使NaNO2转化为不引起二次污染的N2的物质应具有还原性,只有选项B符合,故答案为:B;
(4)Al元素的化合价由0升高为+3价,N元素的化合价由+5价降低为0,该反应还应生成水,由电子守恒及原子守恒可知,反应为10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O,过程中转移5mol e-,则生成标准状况下N2的体积为5mol×$\frac{3}{30}$×22.4L/mol=11.2L,
故答案为:10;6;4;10;3;2H2O;11.2;
(5)①第一步反应中,反应物总能量大于生成物总能量,则该反应为放热反应,△H<0,故答案为:放热;反应物总能量大于生成物总能量;
②1mol NH4+(aq)全部氧化成NO3-(aq)可由两步反应加和得到,热化学方程式为NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol,
故答案为:NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol.
点评 本题考查较综合,涉及氧化还原反应、配平,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应及能量变化的考查,注意从元素化合价角度及图象角度分析,题目难度不大.

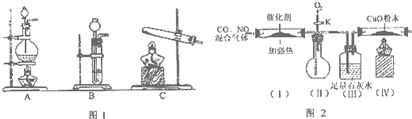
(1)写出用硝酸制取一氧化氮的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)查资料得知,HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+H2O.实验室有如图1所示的装置,制取CO气体可选用的装置为A(填序号),实验室利用该装置还可制取的常见气体有Cl2(填写一种气体的分子式).
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气.该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去).
①实验前关闭旋塞K,先通氮气排净装置中的空气,其目的是防止CO与空气混合加热爆炸
②该套装置中有不完善之处,还应在装置(Ⅳ)后补充尾气处理装置装置.
Ⅱ.该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4•7H2O过程如下:
a.在混合液中加入6mol•L-1NaOH溶液,至pH=8为止.
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀.
c.向洗涤后的沉淀中加入2mol•L-1的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液.
d.滤液中加入2mol•L-1的硫酸,使其pH=2.
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Fe (OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
(2)步骤d中加入硫酸,使其pH=2的目的是抑制Zn2+的水解; 要制得ZnSO4•7H2O的步骤d还缺少的操作是将溶液加热浓缩,冷却结晶.
| A. | 所占硫原子的物质的量之比为1:1 | B. | 氧原子的物质的量之比为2:3 | ||
| C. | 氧元素的质量比为2:3 | D. | 体积比为1:1 |
| A. | 金属钠着火燃烧时,用干燥沙土灭火 | |
| B. | 点燃可燃性气体前,都必须先检验气体的纯度 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液擦洗 | |
| D. | 配制H2SO4溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓H2SO4 |
| A. | Cl2+H2O═HCl+HClO | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | 2F2+2H2O═4HF+O2↑ | D. | CaO+H2O═Ca(OH)2 |
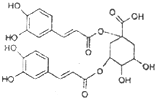 洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )| A. | A在酸性条件下可以发生水解反应 | |
| B. | 1mol A和足量NaOH溶液反应,最多消耗9molNaOH | |
| C. | A能和浓溴水发生加成和取代反应 | |
| D. | 不能与新制得Cu(OH)2反应但能与FeCl3发生显色反应 |
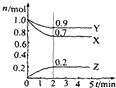 某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析:
某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析: