题目内容
【题目】根据下表中的信息判断,下列说法错误的是
序号 | 反应物 | 产物 |
① | Cl2、H2O2 | Cl-、…… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | KClO3、HCl | Cl2、KCl、H2O |
A.第①组反应的氧化产物为O2
B.第②组反应中C12与FeBr2的物质的量之比小于或等于1:2
C.第③组反应中生成3mol C12,转移6mol电子
D.氧化性由强到弱的顺序为C1O3- >C12>Fe3+
【答案】C
【解析】
A.H2O2中O元素的化合价升高,失去电子,被氧化,则H2O2反应的氧化产物为O2,故A正确;
B.②中溴元素的化合价没有变化,Cl2只将Fe2+氧化为Fe3+,发生的反应为3Cl2+6FeBr2 = 2FeCl3+4FeBr3,则Cl2与FeBr2的物质的量之比为1:2,若小于1:2,也只发生该反应,故B正确;
C.在KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3mol氯气转移5mol电子,生成1molCl2转移![]() mol电子,故C错误;
mol电子,故C错误;
D.KClO3+6HCl=KCl+3Cl2↑+3H2O反应中,物质的氧化性:ClO3->Cl2,Cl2氧化FeBr2生成FeBr3,则氧化性:Cl2>Fe3+,因此物质的氧化性由强到弱的顺序为ClO3->Cl2>Fe3+,故D正确;
综上所述,答案为C。

【题目】某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Fe2+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
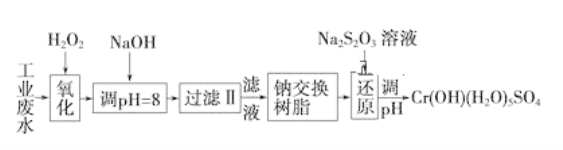
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR→MRn+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+B.Al3+C.Ca2+D.Mg2+
(3)还原过程中,每消耗0.8 mol Cr2O72-转移4.8 mol e-,该反应离子方程式为____________。
【题目】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | N(CO)/mol | N(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是( )
A.反应在t1min内的平均速率为v(H2)=![]() molL-1min
molL-1min
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20mol H2O,达到平衡时n(CO2)=0.40mol
C.保持其他条件不变,向平衡体系中再通入0.20mol H2O,与原平衡相比,达到新平衡时CO转化率不变,H2O的体积分数不变
D.温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应