题目内容
将反应4(NH4)2SO4=N2↑+6 NH3↑+3SO2↑+SO3↑+7H2O的产物气体通入BaCl2溶液,下列判断正确的是
| A.无沉淀生成 |
| B.肯定没有BaSO3生成 |
| C.得到的沉淀是纯净物 |
| D.得到的沉淀是BaSO4和BaSO3组成的混合物 |
D
解析试题分析:根据题意知,将反应后的混合气体通入到BaCl2溶液中发生的反应为:
SO3+H2O+2NH3 =(NH4)2SO4;(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl;SO2+H2O+2NH3=(NH4)2SO3 ;(NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl;结合分解生成的气体物质的量可知,1mol三氧化硫转化为1mol硫酸铵消耗氨气2mol,剩余4mol氨气,4mol氨气会和2mol二氧化硫反应生成2mol亚硫酸铵,2mol亚硫酸铵对应得到2mol亚硫酸钡,剩余1mol二氧化硫和1mol亚硫酸钡、1mol水反应生成1mol亚硫酸氢钡,剩余1mol亚硫酸钡,最后得到沉淀为1mol硫酸钡,1mol亚硫酸钡,因此得到沉淀为BaSO3和BaSO4。选D。
考点:考查二氧化硫和三氧化硫的性质及相关计算。

下列关于浓硝酸和浓硫酸的叙述错误的是( )
| A.和铜反应中都表现出强氧化性和酸性 |
| B.分别露置在空气中,容器内溶质的物质的量浓度都降低 |
| C.都可以储存于铝制槽罐中 |
| D.都是常用的干燥剂 |
下列说法正确的是 ( )
| A.浓硝酸和浓硫酸露置于空气中,容器内酸液的浓度都降低 |
| B.可用铁制容器储存稀硝酸 |
| C.SO2溶于水生成H2SO4 |
| D.SO2通入BaCl2溶液中能产生白色沉淀 |
氯化碘(ICl)的化学性质跟氯气相似,预计它与水反应的最初生成物是( )。
| A.HI和HClO | B.HCl和HIO |
| C.HClO3和HIO | D.HClO和HIO |
有关高温结构陶瓷和光导纤维的说法正确的是( )。
| A.高温结构陶瓷弥补了金属材料的弱点,但是硬度却远远低于金属材料 |
| B.氮化硅陶瓷是一种重要的结构材料,具有超硬性,它不与任何无机酸反应 |
| C.光导纤维是一种能高质量传导光的玻璃纤维 |
| D.光导纤维的抗干扰性能好,不发生电辐射,通讯质量高,能防窃听 |
工业上由粗硅制取高纯硅有以下反应:①Si(s)+3HCl(g)=SiHCl3(g)+H2(g) ΔH=-381 kJ·mol-1;
②SiHCl3(g)+H2(g)=Si(s)+3HCl(g)。对上述反应的说法中正确的是( )。
| A.均为置换反应和氧化还原反应 |
| B.反应①、②实际上互为可逆反应 |
| C.由于反应①放热,则反应②可能是吸热的,也可能是放热的 |
| D.提高SiHCl3产率,应采用加压和升温的办法 |
“神九”飞船上载有活性炭材料的器材,其作用是( )
| A.处理宇航员的生活垃圾 | B.去除呼吸废气中的异味 |
| C.提供生活中需要的能量 | D.改善失重条件下的平衡 |
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O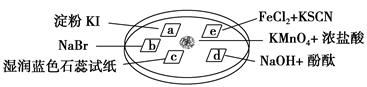
对实验现象的“解释或结论”正确的是 ( )。
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变 红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |