题目内容
19.除去括号中杂质,写出所加试剂与反应的离子方程式.(1)SO42-(CO32-),所加试剂:硫酸,离子方程式:2H++CO32-═H2O+CO2↑.
(2)Cl-(SO42-),所加试剂:氯化钡,离子方程式:Ba2++SO42-═BaSO4↓.
(3)Fe2+(Cu2+),所加试剂:Fe,离子方程式:Fe+Cu2+═Fe2++Cu.
分析 (1)加硫酸可除杂,反应生成水、二氧化碳;
(2)加氯化钡可除杂,硫酸根离子与钡离子结合生成沉淀;
(3)加Fe可除杂,Fe与铜离子反应生成亚铁离子和Cu.
解答 解:(1)加硫酸可除杂,反应生成水、二氧化碳,离子反应为2H++CO32-═H2O+CO2↑,故答案为:硫酸;2H++CO32-═H2O+CO2↑;
(2)加氯化钡可除杂,硫酸根离子与钡离子结合生成沉淀,离子反应为Ba2++SO42-═BaSO4↓,故答案为:氯化钡;Ba2++SO42-═BaSO4↓;
(3)加Fe可除杂,Fe与铜离子反应生成亚铁离子和Cu,离子反应为Fe+Cu2+═Fe2++Cu,故答案为:Fe;Fe+Cu2+═Fe2++Cu.
点评 本题考查离子反应方程式的书写及除杂,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
7.有关金属腐蚀的论述,正确的是( )
| A. | 金属的腐蚀一定伴有电流产生 | |
| B. | Fe在干燥的氯气里比在潮湿的空气里更易被腐蚀 | |
| C. | 发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀 | |
| D. | 发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子 |
14.碘元素有“智力元素”之称.研究性学习小组做了如下实验探究海带中碘元素存在并测定其中碘元素的含量.
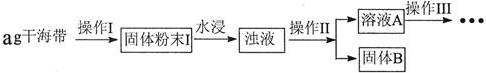
(1)操作Ⅰ为灼烧,则灼烧时用坩埚 盛装海带,操作Ⅱ为过滤
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性,I2+2S2O32-═2I-+S4O62-
将上述溶液稀释配制成200mL溶液,请完成下列实验探究.限选试剂:3%H2O2溶液、KSCN溶液、FeCL2溶液、稀硫酸
(4)定量检验海带中的碘含量:
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4
溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B
②在溶液B加入两滴淀粉溶液,用0.01mol/LNaS2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量$\frac{1.27V}{a}$×100%.
(假设操作Ⅰ、Ⅱ过程中碘不损失,原子量I-127)

(1)操作Ⅰ为灼烧,则灼烧时用坩埚 盛装海带,操作Ⅱ为过滤
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性,I2+2S2O32-═2I-+S4O62-
将上述溶液稀释配制成200mL溶液,请完成下列实验探究.限选试剂:3%H2O2溶液、KSCN溶液、FeCL2溶液、稀硫酸
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 |  |
| ② | 往试管Ⅰ中加入FeCl2溶液后,加入2滴KSCN溶液并振荡 | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4
溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B
②在溶液B加入两滴淀粉溶液,用0.01mol/LNaS2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量$\frac{1.27V}{a}$×100%.
(假设操作Ⅰ、Ⅱ过程中碘不损失,原子量I-127)
4.实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )


| A. | ①是氨气发生装置 | B. | ②是氨气吸收装置 | ||
| C. | ③是氨气发生装置 | D. | ④是氨气收 集、检验装置 |
11.W、X、Y、Z是原子序数依次增大的四种短周期主族元素,W的阳离子能抑制水的电离,X、Z同主族,元素原子最外层电子数Z是Y的2倍,四种元素原子最外层电子数之和为16.下列说法正确的是( )
| A. | Y的最高价氧化物的水化物具有弱酸性 | |
| B. | 阳离子的氧化性:Y>W | |
| C. | 原子半径:Z>Y | |
| D. | 元素W、X、Z各自最高和最低化合价的代数和分别为0、4、4 |
8.下列物质中既有氧化性又有还原性的是( )
| A. | SO3 | B. | Al2O3 | C. | Na2O2 |
9.下列微粒的存在最能说明碘可能呈现还原性的是( )
| A. | I- | B. | I2 | C. | I2+ | D. | I${\;}_{3}^{-}$ |