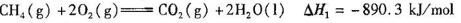题目内容
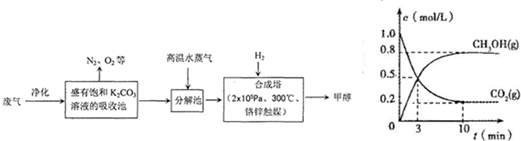
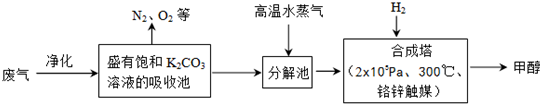
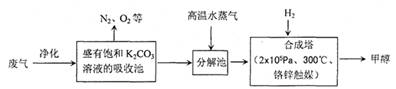
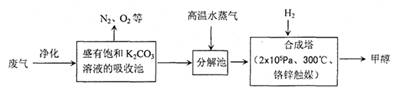
为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇.“绿色自由”构想的部分技术流程如下:

(1)吸收池中主要反应的离子方程式为______,该过程中反应液的pH______(填“增大”、“减小”或“不变”).
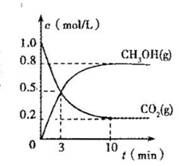
(2)合成塔中反应的化学方程式为______;△H<0.从平衡移动原理分析,低温有利于提高原料气的平衡转化率.而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑______.若反应不使用催化剂,其他条件不变时,△H______(填“增大”、“减小”或“不变”).
(3)从合成塔分离出甲醇的原理与下列______操作的原理比较相符(填字母)
A.过滤 B.分液 C.蒸馏 D.结晶
工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施.“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括______.
(4)若在实验室模拟“绿色自由”构想,则需要制取氢气.现要组装一套可以控制氢气输出速率的装置,则必需选用的下列仪器为______(填字母).
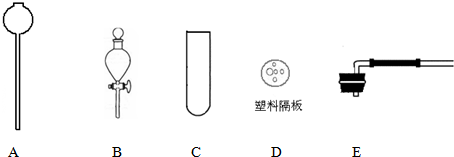
将氢气通入模拟合成塔前必须进行的操作是______.
解:(1)二氧化碳与碳酸钾反应生成碳酸氢钾,反应的离子方程式为CO32-+CO2+H2O=2HCO3-,由于CO32-水解程度大于HCO3-,则溶液pH减小,
故答案为:CO32-+CO2+H2O=2HCO3-;减小;
(2)合成塔反应是二氧化碳和氢气在一定条件下可生成甲醇和水,其方程式为CO2+3H2 CH3OH+H2O,温度影响催化剂的活性,除考虑温度对反应速率的影响外,还主要考虑了催化剂的催化活性,无论是否加入催化剂,反应热都不变,只与反应物与生成物有关,
CH3OH+H2O,温度影响催化剂的活性,除考虑温度对反应速率的影响外,还主要考虑了催化剂的催化活性,无论是否加入催化剂,反应热都不变,只与反应物与生成物有关,
故答案为:CO2+3H2 CH3OH+H2O; 催化剂的催化活性; 不变;
CH3OH+H2O; 催化剂的催化活性; 不变;
(3)从合成塔出来的主要为甲醇与水的混合液,甲醇与水互溶,沸点相差大,可用蒸馏的方法分离,由工艺流程可知,可重复利用的物质有K2CO3溶液和CO2、H2、高温水蒸气,
故答案为:C;高温水蒸气或反应热;
(4)控制氢气输出速率,并且符合绿色自由的构想,应控制酸的用量,减少浪费,可用分液漏斗加入,在试管中进行反应,则应选用BCE,不纯的氢气易爆炸,应先验纯,故答案为:BCE;检验氢气的纯度.
分析:(1)二氧化碳与碳酸钾反应生成碳酸氢钾,起到吸收、提纯二氧化碳的目的,反应后溶液的pH减小;
(2)根据工艺流程可知,合成塔内反应是氢气与二氧化碳反应生成甲醇和水;工业生产条件选择要考虑转化率、反应速率、对催化剂的影响、材料、成本等多方面综合考虑;
(3)从合成塔出来的主要为甲醇与水的混合液,甲醇与水互溶,沸点相差大;由流程图可以找出循环利用的物质;
(4)控制氢气输出速率,并且符合绿色自由的构想,应控制酸的用量,减少浪费,可用分液漏斗加入,在试管中进行反应.
点评:本题通过研究二氧化碳对环境的影响,考查学生分析图示及书写方程式的能力、气体制备实验设计等,解题时首先要根据流程图明确物质的制备过程.
故答案为:CO32-+CO2+H2O=2HCO3-;减小;
(2)合成塔反应是二氧化碳和氢气在一定条件下可生成甲醇和水,其方程式为CO2+3H2
 CH3OH+H2O,温度影响催化剂的活性,除考虑温度对反应速率的影响外,还主要考虑了催化剂的催化活性,无论是否加入催化剂,反应热都不变,只与反应物与生成物有关,
CH3OH+H2O,温度影响催化剂的活性,除考虑温度对反应速率的影响外,还主要考虑了催化剂的催化活性,无论是否加入催化剂,反应热都不变,只与反应物与生成物有关,故答案为:CO2+3H2
 CH3OH+H2O; 催化剂的催化活性; 不变;
CH3OH+H2O; 催化剂的催化活性; 不变;(3)从合成塔出来的主要为甲醇与水的混合液,甲醇与水互溶,沸点相差大,可用蒸馏的方法分离,由工艺流程可知,可重复利用的物质有K2CO3溶液和CO2、H2、高温水蒸气,
故答案为:C;高温水蒸气或反应热;
(4)控制氢气输出速率,并且符合绿色自由的构想,应控制酸的用量,减少浪费,可用分液漏斗加入,在试管中进行反应,则应选用BCE,不纯的氢气易爆炸,应先验纯,故答案为:BCE;检验氢气的纯度.
分析:(1)二氧化碳与碳酸钾反应生成碳酸氢钾,起到吸收、提纯二氧化碳的目的,反应后溶液的pH减小;
(2)根据工艺流程可知,合成塔内反应是氢气与二氧化碳反应生成甲醇和水;工业生产条件选择要考虑转化率、反应速率、对催化剂的影响、材料、成本等多方面综合考虑;
(3)从合成塔出来的主要为甲醇与水的混合液,甲醇与水互溶,沸点相差大;由流程图可以找出循环利用的物质;
(4)控制氢气输出速率,并且符合绿色自由的构想,应控制酸的用量,减少浪费,可用分液漏斗加入,在试管中进行反应.
点评:本题通过研究二氧化碳对环境的影响,考查学生分析图示及书写方程式的能力、气体制备实验设计等,解题时首先要根据流程图明确物质的制备过程.

练习册系列答案
相关题目