题目内容
(14分) 为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下:
(1)合成塔中反应的化学方程式为 ;△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 。
(2)从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)
A.过滤 B.分液 C.蒸馏 D.结晶
工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括 。
(3)一定条件下,向体积为1 L的密闭容器中充入1 molCO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是 。
A.升高温度能使增大
B.反应达到平衡状态时,CO2的平衡转化率为75%
C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol•L-1•min-1
(4) 如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
巳知
写出C02(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式
___________ _____。
(14分)(1)CO2+3H2=CH3OH+H2O(3分) 催化剂的催化活性(2分)
(2)C(2分) 高温水蒸气或反应热(2分) (3)B(3分)
(4) CO2(g)+4H2(g) = CH4(g)+2H2O(l) ΔH=-252.9kJ/mol(3分)
解析:

 阅读快车系列答案
阅读快车系列答案(14分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
⑴“除杂”时先通入足量Cl2将Fe2+氧化成Fe3+,再加入CuO固体调节溶液的pH至 (填写范围)。检验Fe(OH)3是否沉淀完全的实验方案是 。
⑵操作X包括 、 、过滤和洗涤等。CuCl2·3H2O加热灼烧的最终产物的化学式是 。
⑶某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃药于锥形瓶中。
c.向锥形瓶内加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,至达到滴定终点。
e.重复bcd三步的操作2次。
① 操作c中量取盐酸体积的仪器是 。
② 若洗涤后的碱式滴定管未用NaOH溶液润洗,则所测CaCO3的质量分数将 (选填“偏大”、“偏小”或“无影响”)。
③ 若滴定中NaOH溶液的平均用量为15.00mL,则胃药中碳酸钙的质量分数为 。
(14分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下: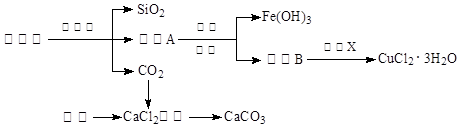
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
⑵操作X包括 、 、过滤和洗涤等。CuCl2·3H2O加热灼烧的最终产物的化学式是 。
⑶某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃药于锥形瓶中。
c.向锥形瓶内加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,至达到滴定终点。
e.重复bcd三步的操作2次。
①操作c中量取盐酸体积的仪器是 。
②若洗涤后的碱式滴定管未用NaOH溶液润洗,则所测CaCO3的质量分数将 (选填“偏大”、“偏小”或“无影响”)。
③若滴定中NaOH溶液的平均用量为15.00mL,则胃药中碳酸钙的质量分数为 。
(14分) CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。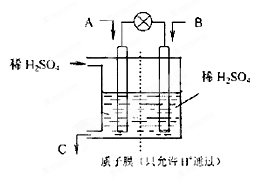
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是 (填序号)
| A.减少化石燃料的使用,开发新能源 |
| B.使用无氟冰箱,减少氟利昂排放 |
| C.多步行或乘公交车,少用私家车 |
| D.将工业废气用碱液吸收后再排放 |
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为 ;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 ;
当电路中有1 mol e-流过,正极区溶液中的H+的物质的量的变化量
 n(H+)= mol。
n(H+)= mol。(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:l7℃、l.01×l05Pa时,2NO2(g)
 N2O4(g) △H<0的平衡常数K=13.3。
N2O4(g) △H<0的平衡常数K=13.3。①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol.L-1,
则c(N2O4)= 。(保留两位有效数字)
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)="0.04" mol.L-1,c(N2O4)="0.007" mol.L-1,则改变的条件为 。
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g)
 CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。 (14分) CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。

(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是 (填序号)
A、减少化石燃料的使用,开发新能源
B、使用无氟冰箱,减少氟利昂排放
C、多步行或乘公交车,少用私家车
D、将工业废气用碱液吸收后再排放
(2)有学者设想以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为 ;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 ;
当电路中有1 mol e-流过,正极区溶液中的H+的物质的量的变化量 n(H+)=
mol。
n(H+)=
mol。
(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:l7℃、l.01×l05Pa时,2NO2(g) N2O4(g)
△H<0的平衡常数K=13.3。
N2O4(g)
△H<0的平衡常数K=13.3。
①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol.L-1,
则c(N2O4)= 。(保留两位有效数字)
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04 mol.L-1,c(N2O4)=0.007 mol.L-1,则改变的条件为 。
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g) CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将
。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将
。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
(14分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:

为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
|
物质 |
pH (开始沉淀) |
pH(完全沉淀) |
|
Fe(OH)3 |
1.9 |
3.2 |
|
Fe(OH)2 |
7.0 |
9.0 |
|
Cu(OH)2 |
4.7 |
6.7 |
⑴“除杂”时先通入足量Cl2将Fe2+氧化成Fe3+,再加入CuO固体调节溶液的pH至 (填写范围)。检验Fe(OH)3是否沉淀完全的实验方案是 。
⑵操作X包括 、 、过滤和洗涤等。CuCl2·3H2O加热灼烧的最终产物的化学式是 。
⑶某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃药于锥形瓶中。
c.向锥形瓶内加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,至达到滴定终点。
e.重复bcd三步的操作2次。
① 操作c中量取盐酸体积的仪器是 。
② 若洗涤后的碱式滴定管未用NaOH溶液润洗,则所测CaCO3的质量分数将 (选填“偏大”、“偏小”或“无影响”)。
③ 若滴定中NaOH溶液的平均用量为15.00mL,则胃药中碳酸钙的质量分数为 。