题目内容
15.下列化学方程式或离子方程式,不正确的是( )| A. | 溴乙烷与氢氧化钠的醇溶液共热:CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O | |
| B. | 用银氨溶液检验乙醛中的官能团:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| C. | 向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 甘氨酸与氢氧化钠溶液反应:H2N-CH2COOH+OH-→H2N-CH2COO-+H2O |
分析 A.卤代烃在氢氧化钠的醇溶液中发生消去反应生成烯烃;
B.乙醛与银氨溶液发生反应生成乙酸铵、银、氨气和水;
C.苯酚的酸性大于碳酸氢根离子,二者反应生成苯酚和碳酸氢根离子;
D.甘氨酸中含有羧基,能够与强氧化钠溶液发生中和反应.
解答 解:A.溴乙烷与氢氧化钠的醇溶液共热发生消去反应生成乙烯,反应的化学方程式为:CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O,故A正确;
B.用银氨溶液检验乙醛中的官能团,反应的离子方程式为:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O,故B正确;
C.向苯酚钠溶液中通入少量的CO2,反应生成苯酚和碳酸氢根离子,正确的离子方程式为:CO2+H2O+C6H5O-→C6H5OH+HCO3-,故C错误;
D.甘氨酸与氢氧化钠溶液反应的离子方程式为:H2N-CH2COOH+OH-→H2N-CH2COO-+H2O,故D正确;
故选C.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确常见的需要保留化学式的物质,如:弱电解质、气体、氧化物、难溶物等,C为易错点,注意苯酚的酸性大于碳酸氢根离子,二氧化碳少量时反应生成碳酸氢根离子.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
10.下列有关烃的衍生物说法中,正确的是( )
| A. | 用钠检验乙醇中含有少量水 | |
| B. | 能与新制氢氧化铜反应的物质一定是乙醛 | |
| C. | 乙酸与乙酸乙酯互为同分异构体 | |
| D. | 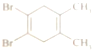 如图所示有机物分子核磁共振氢谱有两个峰 |
20.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了Cu/Zn原电池,该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑
(3)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等(答两种).
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了Cu/Zn原电池,该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑
(3)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等(答两种).
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL-1 | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL-1 | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL-1 | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
7.下列关于有机物的说法中,错误的是( )
| A. | 在一定条件下葡萄糖能与新制Cu(OH)2发生反应 | |
| B. | 肥皂的主要成分是油脂在碱性条件下水解生成的 | |
| C. | 淀粉、纤维素和油脂都是天然高分子化合物 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水 |
4.下列事实可以表明醋酸是弱电解质的是( )
| A. | 醋酸能与水任意比例互溶 | |
| B. | 醋酸溶液的导电能力比盐酸弱 | |
| C. | 醋酸溶液中存在醋酸根离子、氢离子 | |
| D. | 常温下,1 mol•L-1的醋酸中c(H+)约为0.01 mol•L-1 |
5.以下有关元素性质的说法不正确的是( )
| A. | 具有下列电子式的原子中,①1s22s22p63s23p2、②1s22s22p3、③1s22s22p2、④1s22s22p63s23p4,原子半径最大的是① | |
| B. | 下列原子的价电子排布中,①3s23p1②3s23p2③3s23p3④3s23p4对应的第一电离能最大是③ | |
| C. | 某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+ | |
| D. | ①Na、K、Rb,②N、P、As,③O、S、Se,④Na、P、Cl 元素的电负性随原子序数增大而递增的是④ |
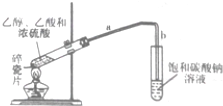 合成乙酸乙酯的路线如下:
合成乙酸乙酯的路线如下: .
.