题目内容
已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2220.0kJ·mol-1
实验测得氢气和丙烷的混和气体共5mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是( )
| A.1:3 | B.3:1 | C.1:4 | D.1:1 |
B
解析试题分析:假定5mol的全部是H2(g),则放出的热量为:1429kJ。假定5mol的全部是C3H8(g),则放出的热量为:11100kJ。现在放出的热量为:3847kJ,则可以用十字相乘法来求出氢气和丙烷的体积比:十字相乘法:1429 7253 3
3847
11100 2418 1
从以上过程可以看出:氢气和丙烷的体积比为:3:1,选B。
考点:考查常识。

 一课一练课时达标系列答案
一课一练课时达标系列答案下列物质性质的变化规律,与共价键的键能大小无关的是( )
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高 ②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石、碳化硅、晶体硅熔点逐渐降低 ④NaF、NaCl、NaBr、NaI的熔点依次降低
| A.仅② | B.①④ | C.②③ | D.①②③ |
下列有关能量转换的说法正确的是( )
| A.煤燃烧是化学能全部转化为热能的过程 |
| B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 |
| D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
下列原理所测的中和热最接近-57.3 kJ/mol的是( )
| A.将标况下11.2L HCl气体通入50mL 0.01 mol/L NaOH溶液中反应 |
| B.用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L HNO3溶液反应 |
| C.用55mL 0.01 mol/L Ba(OH)2溶液与50mL 0.01 mol/L H2SO4溶液反应 |
| D.用55mL 0.01 mol/L NaOH溶液与50mL 0.01 mol/L HF溶液反应 |
已知:
(1)Fe2O3(s) + C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
(2)C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+ O2(g)=Fe2O3(s) 的ΔH是( )
O2(g)=Fe2O3(s) 的ΔH是( )
| A.-824.4 kJ/mol | B.-627.6 kJ/mol |
| C.-744.7 kJ/mol | D.-169.4 kJ/mol |
下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g)= 2H2O(l) ΔH=-571.6 kJ·mol-1,则氢气的燃烧热为285.8 kJ·mol-1 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)= CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。
已知:CH3OH(l)+O2(g)= CO(g)+2H2O(g) 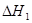 ="-443.64" kJ·mol-1
="-443.64" kJ·mol-1
2CO(g)+ O2(g)= 2CO2(g) 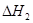 = -566.0kJ·mol-1
= -566.0kJ·mol-1
下列说法或热化学方程式正确的是
| A.CO的燃烧热为566.0 kJ·mol-1 |
| B.2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 |
| C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3 kJ |
D.2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g)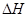 ="-1453.28" kJ·mol-1 ="-1453.28" kJ·mol-1 |
下列说法或表示方法正确的是( )
| A.已知C(s)+O2(g)=CO2(g) ΔH1,C(s)+1/2O2(g)="CO(g)" ΔH2;则ΔH1>ΔH2 |
| B.等量的H2在O2中完全燃烧,生成气态水比生成液态水放出的热量多 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| D.由石墨比金刚石稳定可知:C(金刚石, s)=C(石墨, s) ΔH >0 |
CO(g)+H2O(g) H2(g)+CO2(g)<0,在其他条件不变的情况下:
H2(g)+CO2(g)<0,在其他条件不变的情况下:
| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.若在原电池中进行,反应放出的热量不变 |