题目内容
【题目】现在部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
T | M层上有6个电子 |
Z | 元素最高正价是+7价 |
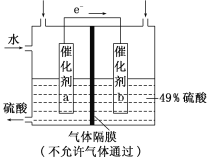
W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
用相应的元素符号或化学式回答以下问题
(1)元素X的一种同位素中子数比质子数多1,这种同位素的符号是______。
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式______。
(3)元素Z与元素T相比,非金属较强的是______(用元素符号表示)。
(4)T、X、Y、Z四种元素的最高价氧化物对应的水化物中酸性最强的是______(化学式)
(5)T的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为______。
【答案】![]()
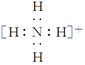 Cl HClO4 Al(OH)3+3H+=Al3++3H2O
Cl HClO4 Al(OH)3+3H+=Al3++3H2O
【解析】
X最外层电子数是次外层电子数的2倍,所以X是碳元素。Y单质常温下为双原子分子,其氢化物的水溶液呈碱性,所以Y是氮元素。T原子M层上有6个电子,故T的质子数为16,T为硫。Z的最高正价是+7价,在短周期中只有氯元素有+7价。W单质既能与酸反应又能跟碱反应都生成氢气,W为铝。
(1)元素C的一种同位素中子数比质子数多1,碳的质子数是6,中子数7,这种同位素的符号是![]() ;
;
(2)N和H形成的NH4+的电子式为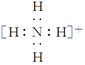 ;
;
(3)Cl得电子能力比S强,所以Cl的非金属性比S强;
(4)C、N、S、Cl这四种元素非金属性最强的是Cl,所以最高价氧化物对应的水化物酸性最强的是高氯酸,故答案为:HClO4;
(5)硫的最高价氧化物对应的水化物为硫酸,铝的最高价氧化物对应的水化物是氢氧化铝,两者发生酸碱中和反应。离子方程式为:Al(OH)3+3H+=Al3++3H2O。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
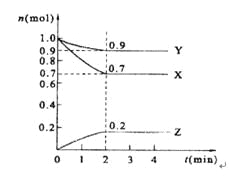
小夫子全能检测系列答案【题目】I. 某可逆反应在某体积为2L的密闭容器中进行,在从0~3min各物质的量的变化情况如图所示(A、B、C均为气体)。

(1)该反应的化学方程式为______。
(2)反应开始至2min时,B的平均反应速率为______。
(3)能说明该反应已达到平衡状态的是______。
A. c(A)= c(B)= c(C) B.容器内压强保持不变
C .v逆(A)= v正(C) D. c(C)不再变化
(4)由图求得A的平衡时的转化率为______。
Ⅱ.(5)已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
共价键 | H—H | N—H | N≡N |
能量变化/kJ·mol-1 | a | b | c |
则合成氨反应:N2(g) + 3H2 (g)= 2NH3(g) ![]() H = ______kJ·mol-1
H = ______kJ·mol-1