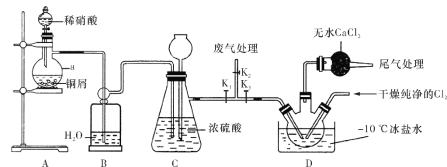
题目内容
【题目】下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是

A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
【答案】B
【解析】
A.该装置没有外加电源,是一个原电池,把化学能转化为电能,故A正确;B.由图示可看出,电子由a表面转移到b表面,因此a表面发生氧化反应,由题意SO2转化为H2SO4发生氧化反应,因此催化剂a表面SO2发生氧化反应,催化剂b表面O2发生还原反应生成H2O,消耗H+,其附近酸性减弱,故B错误;C.催化剂a表面是SO2失去电子生成硫酸,电极方程式为:SO2+2H2O-2e-=SO42-+4H+,故C正确;D.催化剂a处的反应为:SO2+2H2O-2e-=SO42-+4H+,催化剂b处的反应为:![]() O2+2H++2e-=H2O,总方程为:SO2+H2O+
O2+2H++2e-=H2O,总方程为:SO2+H2O+![]() O2=H2SO4,设加入的SO2为xg,H2O为yg。则生成硫酸的质量为:
O2=H2SO4,设加入的SO2为xg,H2O为yg。则生成硫酸的质量为:![]() =
=![]() g,水的质量变化为:y-
g,水的质量变化为:y-![]() =(y-
=(y-![]() )g,根据硫酸浓度仍为49%,则
)g,根据硫酸浓度仍为49%,则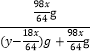 =49%,可以求得
=49%,可以求得![]() =
=![]() ,故D正确;故选B。
,故D正确;故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】现在部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
T | M层上有6个电子 |
Z | 元素最高正价是+7价 |
W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
用相应的元素符号或化学式回答以下问题
(1)元素X的一种同位素中子数比质子数多1,这种同位素的符号是______。
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式______。
(3)元素Z与元素T相比,非金属较强的是______(用元素符号表示)。
(4)T、X、Y、Z四种元素的最高价氧化物对应的水化物中酸性最强的是______(化学式)
(5)T的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为______。