题目内容
12.下列各组物质中,组内各种物质不都属于有机物的是( )| A. | CH4、C2H6O、CH3Cl | B. | C100H202、C6H6、C2H2 | ||
| C. | H2O2、CH4、C2H6 | D. | C2H4、CH4、C6H5NO2 |
分析 根据含有碳元素的化合物叫有机化合物,简称有机物;碳的氧化物、碳酸盐、碳酸氰化物,氰酸盐虽含碳,但其性质与无机物类似,因此把它们看作无机物;据此进行分析判断.
解答 解:A.CH4、C2H6O、CH3Cl是含碳的化合物,属于有机物,故A错误;
B.C100H202、C6H6、C2H2是含碳的化合物,属于有机物,故B错误;
C.H2O2不含碳元素,属于无机物,故C正确;
D.C2H4、CH4、C6H5NO2是含碳的化合物,属于有机物,故D错误.
故选C.
点评 本题考查有机物的概念,难度不大,掌握有机物与无机物的概念、特征等是正确解答此类题的关键.

练习册系列答案
相关题目
13.有两种金属的合金10.5克,与足量稀硫酸反应后,产生的气体在标况下占体积11.2L,则组成该合金的元素可能是( )
| A. | Mg和Al | B. | Fe和Zn | C. | Mg和Cu | D. | Na和Zn |
7.已知铁离子,氯气、溴均为常见的氧化剂,某化学兴趣小组设计了如下实验探究其强弱:
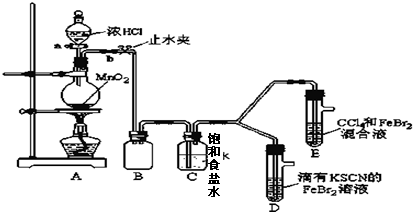
(1)①装置A中发生反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;△\;}}{\;}$Mn2++Cl2↑+2H2O.②整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
(2)用改正后的装置进行实验,实验过程如下:
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化.
D装置中:红色慢慢褪去.
E装置中:CCl4层颜色逐渐加深,直至变成红色.
为探究上述实验现象的本质,小组同学查得资料如下:
①请用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-?Fe(SCN)3平衡向逆反应方向移动而褪色.
现设计简单实验证明上述解释:取少量褪色后的溶液,滴加KSCN溶液溶液,若溶液颜色变红色.则上述解释是合理的.
小组同学另查得资料如下:
②欲探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合上述资料用两步离子方程式解释仅产生白色沉淀原因BrCl+H2O=HBrO+H++Cl-、Ag++Cl-=AgCl↓.

(1)①装置A中发生反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;△\;}}{\;}$Mn2++Cl2↑+2H2O.②整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
(2)用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后 关闭活塞a,点燃酒精灯. (填具体实验操作) | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,下层CCl4层无明显变化.一段时间后CCl4层由无色变为橙色.(填实验现象) | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: Cl2>Br2>Fe3+ |
D装置中:红色慢慢褪去.
E装置中:CCl4层颜色逐渐加深,直至变成红色.
为探究上述实验现象的本质,小组同学查得资料如下:
| ⅰ.Fe3++3SCN-?Fe(SCN)3 是一个可逆反应. ⅱ.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2. |
现设计简单实验证明上述解释:取少量褪色后的溶液,滴加KSCN溶液溶液,若溶液颜色变红色.则上述解释是合理的.
小组同学另查得资料如下:
| ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点约5℃,它与水能发生水解反应,且该反应为非氧化还原反应. ⅳ.AgClO、AgBrO均可溶于水. |
17.下列实验现象的描述错误的是( )
| A. | 红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒 | |
| B. | 钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 | |
| C. | 氢气在氯气中安静燃烧,生成白烟 | |
| D. | 点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 |
2.下列关于能源和作为能源的物质的叙述中错误的是( )
| A. | 化石能源物质内部蕴储着大量的能量 | |
| B. | 绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 | |
| C. | 物质的化学能可以在不同条件下转为热能、电能为人类所利用 | |
| D. | 我国经济发展要全部依靠化石能源 |


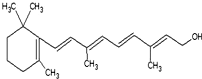 (1)重要的饱和一元脂肪醛有甲醛,其质量分数在35%~40%的水溶液俗称福尔马林.化学性质与乙醛相似,能被氢气还原成甲醇,能被O2、高锰酸钾酸性溶液、溴水、银氨溶液、新制的Cu(OH)2氧化,写出乙醛与银氨溶液反应的方程式CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O.
(1)重要的饱和一元脂肪醛有甲醛,其质量分数在35%~40%的水溶液俗称福尔马林.化学性质与乙醛相似,能被氢气还原成甲醇,能被O2、高锰酸钾酸性溶液、溴水、银氨溶液、新制的Cu(OH)2氧化,写出乙醛与银氨溶液反应的方程式CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O.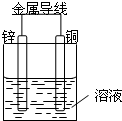 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题: