题目内容
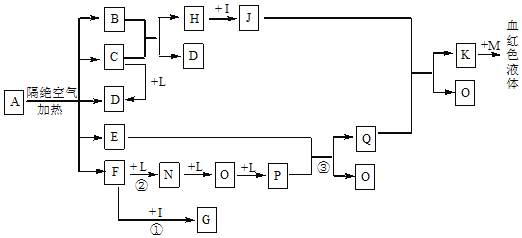
【题目】已知A为一种盐,C、D、F、N、O在常温常压下均为无色气体,E在常温常压下为无色、无味的液体,N、H、L为高中常见的单质,I为常见的无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
(1)写出D的电子式:___;
(2)写出反应②的化学方程式:___;
(3)已知B中氧元素的质量分数为22.2%,且A分解产生的各物质的物质的量之比为n(B):n(C):n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为:___。
【答案】![]() 4NH3+3O2
4NH3+3O2![]() 2N2+6H2O (NH4)2Fe(C2O4)2
2N2+6H2O (NH4)2Fe(C2O4)2
【解析】
E在常温常压下为无色、无味的液体,则E为H2O;I为常见的无氧强酸,则为盐酸;常用浓盐酸检验气体F,则F为NH3;则L为O2,N为N2,O为NO,P为NO2,Q为HNO3;K为Fe(NO3)3,J为FeCl2,H为Fe,B为FeO(由B中氧元素的质量分数为22.2%进行计算),C为CO,D为CO2。
(1)由以上分析知,为![]() ,电此可写出其电子式。
,电此可写出其电子式。
![]() 反应
反应![]() 是氨气氧化生成氮气,由此可写出化学反应方程式。
是氨气氧化生成氮气,由此可写出化学反应方程式。
![]() 在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:
在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:![]() :2:2:1:2,由原子守恒和化合价代数和为0,结合推断中生成物的性质推断出A的化学式为
:2:2:1:2,由原子守恒和化合价代数和为0,结合推断中生成物的性质推断出A的化学式为
通过上面分析,可推知,E为H2O,I为盐酸,F为NH3;L为O2,N为N2,O为NO,P为NO2,Q为HNO3;K为Fe(NO3)3,J为FeCl2,H为Fe,B为FeO,C为CO,D为CO2。
![]() 为
为![]() ,电子式为
,电子式为![]() 。答案为:
。答案为:![]() 。
。
![]() 反应
反应![]() 是氨气的氧化,反应的化学反应方程式为
是氨气的氧化,反应的化学反应方程式为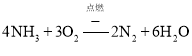 。
。
答案为: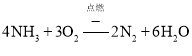 ;
;
![]() 在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:
在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:![]() :2:2:1:2,即FeO:CO:
:2:2:1:2,即FeO:CO:![]() :
:![]() :
:![]() :2:2:1:2,由原子守恒和化合价代数和为0,结合推断中生成物的性质推断出A的化学式为
:2:2:1:2,由原子守恒和化合价代数和为0,结合推断中生成物的性质推断出A的化学式为![]() 。
。
答案为:![]() 。
。