题目内容
14.下列分子中所有原子都满足最外层8电子结构的是( )| A. | 光气(COCl2) | B. | 六氟化硫 | C. | 三氯化硼 | D. | 五氯化磷 |
分析 分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断.
解答 解:A、光气(COCl2)中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,所以满足最外层8电子结构;O原子的原子核外最外层电子数为6,其在分子中的化合价为-2价,所以满足最外层8电子结构;Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,所以满足最外层8电子结构,故A正确;
B、六氟化硫中,S原子的原子核外最外层电子数为6,其在分子中的化合价为+6价,在分子中的原子最外层电子数为12,故B错误;
C、三氟化硼中,B原子的原子核外最外层电子数为3,其在分子中的化合价为+3价,在分子中的原子最外层电子数为6,故C错误;
D、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故D错误.
故选A.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
相关题目
2.短周期元素X、Y、Z、W的原子序数依次增大.X的原子半径比Y的小,且X与Y的最外层电子数之和等于Z的最外层电子数.X与W同主族,Z是地壳中含量最高的元素.下列说法不正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Y)>r(Z)>r(X) | |
| B. | 元素Z、W的简单离子的电子层结构相同 | |
| C. | 元素Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | X、Y两种元素可形成分别含有10e-和18e-的化合物 |
9.某中药的有效成分M具有消炎杀菌作用,M的结构如图所示: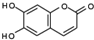 已知
已知 和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )
和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )
 已知
已知 和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )
和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )| A. | M的相对分子质量是180 | |
| B. | 1mol M最多能与2molBr2发生反应 | |
| C. | 1molM与足量的NaOH溶液发生反应,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |
19.已知2NO2 (棕红色)═N2O4(无色).在某支针简中抽入10mlNO2气体并封闭尖端,快速将活塞推至5ml处,其颜色变化是( )
| A. | 变深 | B. | 变浅 | C. | 先变深后变浅 | D. | 先变浅后变深 |
6.在标准状况下,将22.4L NO2通入过量的NaHCO3溶液中,再使逸出的气体通过装有足量Na2O2颗粒的干燥管,最后收集到的气体是( )
| A. | O2 | B. | CO2和O2 | C. | NO2和O2 | D. | NO |
4.下列是某学生自己总结的一些规律,其中正确的是( )
| A. | 一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 | |
| B. | 阳离子只能得到电子被还原,只能做氧化剂 | |
| C. | 含有最高价元素的化合物不一定有强的氧化性 | |
| D. | 氧化物不可能是还原产物,只可能是氧化产物 |
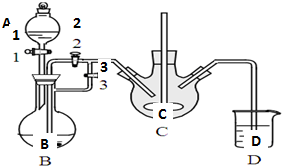 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得: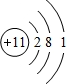 ;
;