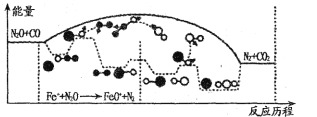
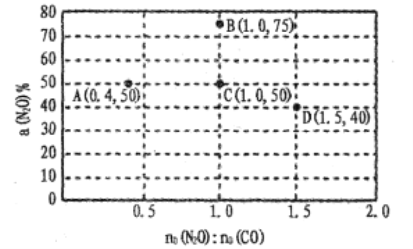
题目内容
【题目】已知:①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH1 ②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2 下列推断正确的是( )
A.若CO的燃烧热为ΔH3,则H2的燃烧热为ΔH3-ΔH1
B.反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=ΔH1-ΔH2
C.若反应②的反应物总能量低于生成物总能量,则ΔH2<0
D.若等物质的量的CO和H2完全燃烧生成气态产物时前者放热更多,则ΔH1<0
【答案】D
【解析】
A.若CO的燃烧热为ΔH3,则③CO(g)+![]() O2(g)=CO2(g) ΔH3,③-①,整理可得H2(g)+
O2(g)=CO2(g) ΔH3,③-①,整理可得H2(g)+![]() O2(g)=H2O(g) ΔH=ΔH3-ΔH1,由于H2O的稳定状态是液态,因此该反应不能表示氢气的燃烧热,A错误;
O2(g)=H2O(g) ΔH=ΔH3-ΔH1,由于H2O的稳定状态是液态,因此该反应不能表示氢气的燃烧热,A错误;
B.①-②,整理可得CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=ΔH2-ΔH1,B错误;
C.若反应②的反应物总能量低于生成物总能量,则该反应是吸热反应,ΔH2>0,C错误;
D.③CO(g)+![]() O2(g)=CO2(g) ΔH3, ④H2(g)+
O2(g)=CO2(g) ΔH3, ④H2(g)+![]() O2(g)=H2O(g) ΔH4,若等物质的量的CO和H2完全燃烧生成气态产物时前者放热更多,则ΔH3<ΔH4,③-④,整理可得CO(g)+H2O(g)=CO2(g)+H2(g) ΔH1=ΔH3-ΔH4<0,D正确;
O2(g)=H2O(g) ΔH4,若等物质的量的CO和H2完全燃烧生成气态产物时前者放热更多,则ΔH3<ΔH4,③-④,整理可得CO(g)+H2O(g)=CO2(g)+H2(g) ΔH1=ΔH3-ΔH4<0,D正确;
故合理选项是D。

【题目】有机化工中3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33 ~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)1mol间苯三酚完全燃烧需要_____molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是________。
②萃取用到的分液漏斗分液时有机层在分液漏斗的____填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是__________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_________(填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)写出反应中可能出现的副产物结构简式______________(只要写一种即可)。