题目内容
16.某原子的原子核外最外层电子排布为ns2np4,按照共用电子对理论,该原子一般可形成共用电子对的数目是( )| A. | 1对 | B. | 2对 | C. | 3对 | D. | 4对 |
分析 原子的原子核外最外层电子排布为ns2np4,形成8电子稳定结构,需要2个电子,以此解答.
解答 解:原子的原子核外最外层电子排布为ns2np4,形成8电子稳定结构,需要2个电子,如形成单键,则可形成共用电子对的数目是2,故选B.
点评 本题考查原子结构与元素的性质,注意元素共价键与原子核外电子排布的关系,难度不大,把握相关规律.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
6.下列化学方程式错误的是( )
| A. |  | |
| B. | 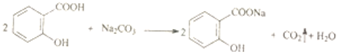 | |
| C. | 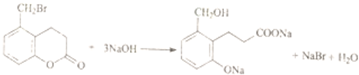 | |
| D. | 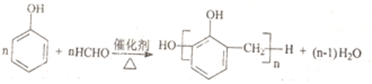 |
7.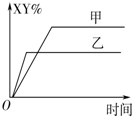 在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
 在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )| A. | 可能是减小了反应物的浓度,反应物X2转化率一定减小 | |
| B. | 可能是加入了催化剂,反应物X2百分含量(X2%)将增大 | |
| C. | 可能是缩小了容器的体积,但该反应的平衡常数保持不变 | |
| D. | 可能是升高了温度,该反应的平衡常数一定减小 |
4.下列有机物命名正确的是( )
| A. | 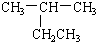 2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2CH2CH2OH 1-丁醇 | ||
| C. |  间二甲苯 间二甲苯 | D. | 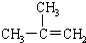 2-甲基-2-丙烯 2-甲基-2-丙烯 |
1.下列图象是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的图象是( )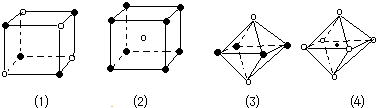

| A. | 图1和图3 | B. | 图2和图3 | C. | 图1 和图4 | D. | 只有 图1 |
8.下列说法中正确的是( )
| A. | 由Fe、Cu、FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-═Cu2+ | |
| B. | 由Al、Mg、NaOH 溶液组成的原电池中,负极反应式为:Al+4OH--3e-═AlO2-+2H2O | |
| C. | 由Al、Cu、稀硫酸溶液组成的原电池中,负极反应式为:Cu-2e-═Cu2+ | |
| D. | 由Al、Cu、浓硝酸溶液组成的原电池中,负极反应式为:Al-3e-═Al3+ |
6.下列各组物质中属于同系物的是( )
| A. | 淀粉和纤维素 | B. | 油酸和丙烯酸 | ||
| C. | 三乙酸甘油酯和硬脂酸甘油酯 | D. | 甲酸乙酯、丙酸 |
 实验室通过加热氯化铵和消石灰来制取氨气.
实验室通过加热氯化铵和消石灰来制取氨气.