题目内容
SO2是大气污染物之一,为粗略地测定周围环境中二氧化硫的含量,某学生课外活动小组设计了如下实验装置: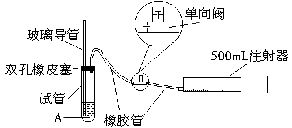
(1)检验该装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后_______________(填写操作方法)时,将会看到__________(填写实验现象),则证明该装置的气密性良好。
(2)向该试管中加入0.0005mol?L-1的碘水1.0mL,加入适量的蒸馏水稀释后再加入2~3滴淀粉溶液,配制成溶液A。测定指定地点的空气中二氧化硫的含量时,推拉注射器的活塞反复抽气,当溶液由______色变为_______色时反应恰好完全进行,此时停止抽气,该反应的化学方程式为____________。
(3)我国环境空气质量标准对每次空气质量测定中二氧化硫的最高浓度的限值如下表:
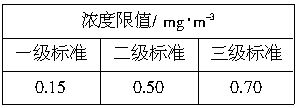
该学生课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,在同一地点、同一时间测量空气中二氧化硫的含量。当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL)。请将下表填写完整(计算时保留两位有效数字):
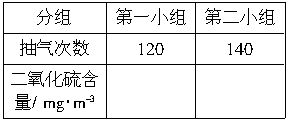
判断该地点的空气中二氧化硫的含量属于___________级标准,______(填“第一”或“第二”)小组的测定结果准确,另一小组实验结果产生较大偏差的原因是(两个小组所用装置和药品均无问题)___________。
见解析
【试题分析】
本题是一道以生产实际问题为素材的实验试题。尽管这个装置及实验方法课本上没有直接出现,但可以用中学化学基础知识进行解答。本题一是容易使有些同学忽视装置左端的玻璃导管与大气相通这一点,而马上用一般的方法检验装置的气密性;二是有些同学实验基本操作不过关,不理解单向阀的原理及作用;三是有些同学被装置的复杂性吓倒,认为这道题目肯定很难,不去仔细分析题中信息就轻易放弃。
(1)向外轻轻拉动注射器的活塞,如果装置气密性良好,装置内压强会减小,空气只能通过玻璃导管进入装置,则浸没在水中的玻璃导管口有气泡冒出。注意轻轻拉,如果猛拉即使装置漏气也会有气泡产生。
(2)二氧化硫和碘反应完全,溶液蓝色褪去变成无色,其反应为SO2+I2+2H2O=H2SO4+2HI。
(3)根据化学方程式可知,反应的二氧化硫的物质的量等于碘的物质的量,第一小组所测空气中二氧化硫的含量为:
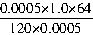 =0.53(mg?m-3)
=0.53(mg?m-3)同理可得第二小组所测空气中二氧化硫的含量为:
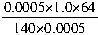 =0.46(mg?m-3)
=0.46(mg?m-3)第一小组抽气次数少,第二小组抽气次数多,而两个小组所用装置和药品均无问题,肯定是操作问题。如果抽气速率过快,就会造成空气中的二氧化硫无法与碘水充分反应,产生较大的误差。所以第一小组的操作正确,因为0.53大于0.50,故此处空气等级应该是三级。

练习册系列答案
相关题目

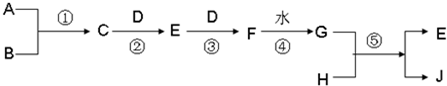

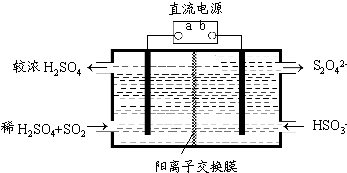
 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。