题目内容
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
(1)若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为______升(标准状况).
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙______克.
(3)若将7.1g氯气用氢氧化钠溶液完全吸收,需消耗0.5mol/L NaOH溶液的体积为______mL.
(1)若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为______升(标准状况).
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙______克.
(3)若将7.1g氯气用氢氧化钠溶液完全吸收,需消耗0.5mol/L NaOH溶液的体积为______mL.
(1)设电解234g氯化钠生成氯气的体积为V,则
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
117 22.4L
234g V
V=44.8L
故答案为:44.8;
(2)设2 mol的氯气通入足量石灰乳中生成次氯酸钙质量为m,则
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
2 143
2mol m
m=143g;
故答案为:143;
(3)7.1g氯气的物质的量为0.1mol,设需要氢氧化钠的物质的量为n,则
2NaOH+Cl2=NaCl+NaClO+H2O
2 1
n 0.1mol
n=0.2mol;
氢氧化钠溶液体积=
=
=0.4L=400ml;
故答案为:400.
2NaCl+2H2O
| ||
117 22.4L
234g V
V=44.8L
故答案为:44.8;
(2)设2 mol的氯气通入足量石灰乳中生成次氯酸钙质量为m,则
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
2 143
2mol m
m=143g;
故答案为:143;
(3)7.1g氯气的物质的量为0.1mol,设需要氢氧化钠的物质的量为n,则
2NaOH+Cl2=NaCl+NaClO+H2O
2 1
n 0.1mol
n=0.2mol;
氢氧化钠溶液体积=
| n |
| c |
| 0.2mol |
| 0.5mol/L |
故答案为:400.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
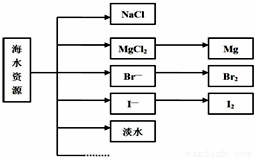
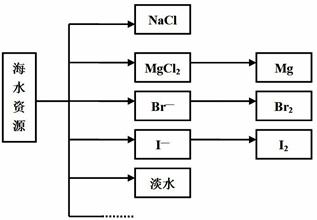
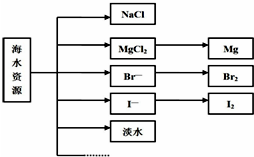 海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.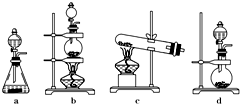
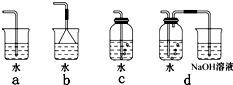
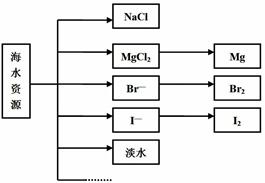
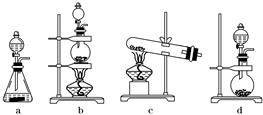
 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 

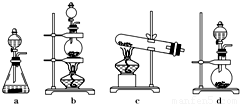
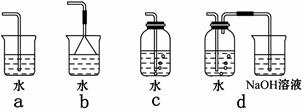
 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。

 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气