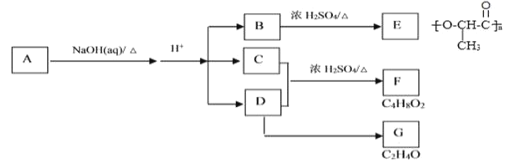
题目内容
【题目】关于下列图示的说法正确的是( )
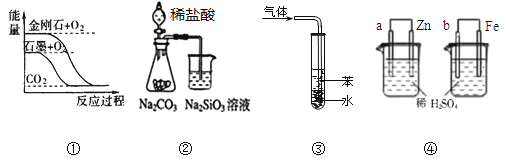
A.图①表示石墨转变为金刚石是吸热反应
B.图②所示实验可比较非金属性强弱:氯﹥碳﹥硅
C.图③吸收NH3并防倒吸
D.图④两装置中金属电极a、b都有气体产生,可判断金属活动性:a﹤b
【答案】A
【解析】
A.图①中1mol金刚石和1molO2的能量比1mol石墨和1molO2的能量高,所以1 mol金刚石的能量比1mol石墨的能量高,石墨转变为金刚石是吸热反应,A正确;
B.图②稀盐酸易挥发,盐酸与硅酸钠反应产生硅酸沉淀,不能比较C、Si非金属性的强弱,且盐酸不是Cl的最高价氧化物的水化物,不能比较Cl、C非金属性的强弱,B错误;
C.图③中导管伸到水面以下,不能防倒吸,C错误;
D.图④中,产生气体(H2)的电极为正极,a、b都为正极,但不能比较二者金属活动性,D错误;
答案选A。

【题目】下列实验操作、现象、得出的结论均正确的是
选项 | 实验操作和现象 | 结论 |
A | 某溶液 | 原溶液中一定含有CO32- |
B | 用湿润的pH试纸测某碱液的pH,测定值偏小 | 湿润的pH试纸测量任何溶液都会产误差 |
C | 将浓硫酸倒入蔗糖中搅拌蔗糖迅速变黑并伴有刺激性气味 | 浓硫酸具有脱水性和强氧化性 |
D | 将乙烯和苯分别加入到溴水中,都能使溴水层褪色 | 乙烯和苯分子中都含有碳碳双键 |
A. A B. B C. C D. D
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
(1)可以判断该分解反应已经达到化学平衡的是____________(填字母序号)。
A.![]() (NH3)=2
(NH3)=2![]() (CO2) B.密闭容器中总压强不变
(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变D.密闭容器气体的平均摩尔质量不变
(2)根据表中数据,列式计算25.0℃时的分解平衡常数____________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,平衡时氨气的浓度____________(填“增加”、“减小”或“不变”)。
(4)氨基甲酸铵分解反应的焓变△H____________0,熵变△S____________0(填“>”、“=”或“<”)该反应在____________条件下有利于其自发进行。
【题目】某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
装置 | 编号 | 电极A | 溶液B | 操作及现象 |
| Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
编号 | 溶液B | 操作及现象 |
Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是____________。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________。