题目内容
20.下列判断错误的是( )| A. | 稳定性:NH3>PH3>AsH3 | B. | 原子半径:N>P>As | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
分析 A.非金属性越强,对应氢化物越稳定;
B.电子层越多,原子半径越大;
C.非金属性越强,对应最高价含氧酸的酸性越强;
D.金属性越强,对应碱的碱性越强.
解答 解:A.非金属性N>P>As,对应氢化物的稳定性为NH3>PH3>AsH3,故A正确;
B.电子层越多,原子半径越大,则原子半径为As>P>N,故B错误;
C.非金属性Cl>S>P,对应最高价含氧酸的酸性为HClO4>H2SO4>H3PO4,故C正确;
D.金属性Na>Mg>Al,对应碱的碱性为NaOH>Mg(OH)2>Al(OH)3,故D正确;
故选B.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
15.自然界为人类提供了多种多样的营养物质,下列有关营养物质的说法正确的是( )
| A. | 麦芽糖、淀粉、纤维素都可以发生水解反应 | |
| B. | 食用纤维素、蛋白质、脂肪和植物油都是高分子化合物 | |
| C. | 棉花和蚕丝的主要成份都是纤维素 | |
| D. | 油脂都不能使溴水褪色 |
11.下列各组的电极材料和电解液,能组成原电池的是( )
| A. | 锌片、石墨棒,稀硫酸 | B. | 铜片、银片,稀盐酸 | ||
| C. | 锌片、铜片,CCl4 | D. | 铁片、铁片,稀硫酸 |
8.已知维生素A的结构简式如图所示,关于它的说法正确的是( )


| A. | 维生素A是一种酚 | |
| B. | 维生素A具有环己烷的结构单元 | |
| C. | 维生素A的一个分子中有3个双键 | |
| D. | 维生素A的一个分子中有30个氢原子 |
15.25℃时,下列有关曲线与对应的叙述正确的是( )
| A. |  表示不同温度下,水溶液中H+和OH-的浓度变化,温度a>b | |
| B. |  表示30%H2O2在60℃时分解率与pH关系,说明pH越大H2O2分解率越大 | |
| C. | 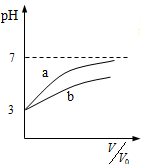 表示体积均为V0、pH均为3的盐酸和醋酸稀释时的pH变化,a表示盐酸 | |
| D. |  是等浓度NaCl和NaI溶液分别用AgNO3溶液滴定,则Ksp(AgI)>Ksp(AgCl) |
5.反应C(s)+H2O(g)?CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,
能够成立的是( )
能够成立的是( )
| A. | 其他条件不变仅将容器的体积缩小一半,反应速率减小 | |
| B. | 保持体积不变,当混合气体密度不变时,反应达到平衡状态 | |
| C. | 保持体积不变,充入少量He使体系压强增大,反应速率一定增大 | |
| D. | 其他条件不变,适当增加C(s)的质量会使反应速率增大 |
12.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. |  用装置制备少量氨气 | B. |  用装置从碘的CCl4溶液中分离出碘 | ||
| C. |  用装置完成喷泉实验 | D. |  用装置蒸发氯化铁溶液制备氯化铁 |
8. 25℃时,向盛有60mL pH=4HA溶液的绝热容器中加入pH=13的NaOH溶液,所得混合溶液的温度(T)与加入NaOH溶液体积(V)的关系如图所示.下列叙述不正确的是( )
25℃时,向盛有60mL pH=4HA溶液的绝热容器中加入pH=13的NaOH溶液,所得混合溶液的温度(T)与加入NaOH溶液体积(V)的关系如图所示.下列叙述不正确的是( )
 25℃时,向盛有60mL pH=4HA溶液的绝热容器中加入pH=13的NaOH溶液,所得混合溶液的温度(T)与加入NaOH溶液体积(V)的关系如图所示.下列叙述不正确的是( )
25℃时,向盛有60mL pH=4HA溶液的绝热容器中加入pH=13的NaOH溶液,所得混合溶液的温度(T)与加入NaOH溶液体积(V)的关系如图所示.下列叙述不正确的是( )| A. | HA溶液的物质的量浓度为0.067mol•L-1 | |
| B. | 25℃时,HA的电离平衡常数约为1.5×10-9 | |
| C. | a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+) | |
| D. | b点时:c(Na+)>c(A-)>c(OH-)>c(H+) |

 .
. ;所属反应类型酯化或取代反应.
;所属反应类型酯化或取代反应. .
. .
.