题目内容
2.有下列两个反应:a.C2H2(g)+H2(g)═C2H4(g)△H<0b.2CH4(g)═C2H4(g)+2H2(g)△H>0.根据上述变化,判断以下几个热化学方程式:
①C(s)+2H2(g)═CH4(g)△H=-$\frac{1}{2}$Q1 kJ/mol
②2C(s)+H2(g)═C2H2(g)△H=-Q2 kJ/mol
③2C(s)+2H2(g)═C2H4(g)△H=-Q3 kJ/mol,其中Q1、Q2、Q3从大到小的顺序是( )
| A. | Q1>Q3>Q2 | B. | Q1>Q2>Q3 | C. | Q2>Q1>Q3 | D. | Q3>Q2>Q1 |
分析 先根据温度变化,平衡移动判断反应a、反应b的热效应,得到焓变符号,根据
(1)C(s)+2H2(g)?CH4(g)△H=-$\frac{1}{2}$Q1 kJ/mol
(2)2C(s)+H2(g)?C2H2(g)△H=-Q2 kJ/mol
(3)2C(s)+2H2(g)?C2H4(g)△H=-Q3 kJ/mol
(3)-(2),得到C2H2(g)+H2(g)?C2H4(g)△H=Q2-Q3,然后利用盖斯定律判断.
解答 解:当温度降低时,反应a的平衡向正反应方向移动,说明该反应正向为放热反应,△H<0,反应b的平衡向逆反应方向移动,说明该反应正向为吸热反应,△H>0,
(1)C(s)+2H2(g)?CH4(g)△H=-$\frac{1}{2}$Q1 kJ/mol
(2)2C(s)+H2(g)?C2H2(g)△H=-Q2 kJ/mol
(3)2C(s)+2H2(g)?C2H4(g)△H=-Q3 kJ/mol
利用盖斯定律,(3)-(2),得到C2H2(g)+H2(g)?C2H4(g)△H=Q2-Q3,与题干中的a中的方程式一样,而a中的反应为放热反应,则Q2-Q3<0,所以Q2<Q3;
同理:(3)-(1)×2,得到2CH4(g)?C2H4(g)+2H2(g)△H=Q1-Q3,与题干中的b中的方程式一样,而b中的反应为吸热反应,则Q1-Q3>0,所以Q1>Q3;
综上所述Q1>Q3>Q2.故选:A.
点评 本题主要考查了盖斯定律的运用,难度不大,根据所学知识即可完成.

练习册系列答案
相关题目
12.在2L恒容密闭容器中发生如图甲的反应.下列判断正确的是( )
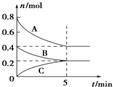

| A. | 5min的时A的转化率为50% | |
| B. | 化学反应方程式为:3A(g)+2B(g)?2C(g) | |
| C. | 降低温度,化学反应速率减小,活化分子百分数不变 | |
| D. | 反应从开始到5min的平均速率v(B)=0.04 mol•L-1•min-1 |
13.下列有关胶体知识叙述正确的组合是( )
①水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
②胶体区别于其他分散系的本质特征是分散质颗粒直径大小
③区分胶体和其他分散系的最简便方法是利用丁达尔效应
④往Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解
⑤医院里用血液透析的方法治疗肾功能衰竭等疾病引起的血液中毒
⑥FeCl3溶液和小苏打溶液混合会产生红褐色沉淀和无色气体
⑦同一支钢笔先后吸入不同牌子的墨水易造成钢笔堵塞
⑧胶体具有介稳性的主要原因是胶体粒子可以通过吸附而带有电荷,且同种胶体粒子的电性相同
⑨在Fe(OH)3胶体中,Fe(OH)3胶体粒子的数目要远远小于原FeCl3溶液中Fe3+的数目.
①水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
②胶体区别于其他分散系的本质特征是分散质颗粒直径大小
③区分胶体和其他分散系的最简便方法是利用丁达尔效应
④往Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解
⑤医院里用血液透析的方法治疗肾功能衰竭等疾病引起的血液中毒
⑥FeCl3溶液和小苏打溶液混合会产生红褐色沉淀和无色气体
⑦同一支钢笔先后吸入不同牌子的墨水易造成钢笔堵塞
⑧胶体具有介稳性的主要原因是胶体粒子可以通过吸附而带有电荷,且同种胶体粒子的电性相同
⑨在Fe(OH)3胶体中,Fe(OH)3胶体粒子的数目要远远小于原FeCl3溶液中Fe3+的数目.
| A. | ①②③④⑦⑥⑧ | B. | ①②④⑤⑦⑧⑨ | C. | ①③④⑤⑦⑧ | D. | ①②③④⑤⑦⑧⑨ |
10.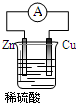 下列关于如图所示装置叙述正确的是( )
下列关于如图所示装置叙述正确的是( )
 下列关于如图所示装置叙述正确的是( )
下列关于如图所示装置叙述正确的是( )| A. | 铜片质量逐渐减小 | B. | H+在铜片表面被还原 | ||
| C. | 电流从锌片经过导线流向铜片 | D. | 铜是负极,铜片上有气泡产生 |
7.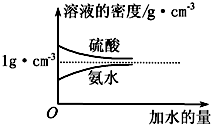 已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,相关数据如表所示.
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,相关数据如表所示.
请根据表中信息,回答下列问题:
(1)表中硫酸的质量分数w1为$\frac{98{c}_{1}}{1000{ρ}_{1}}$(不写单位,用含c1、ρ1的代数式表示);
(2)物质的量浓度为c1 mol•L-1,质量分数为w1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1,质量分数>$\frac{{w}_{1}}{2}$(填“>”、“<”或“=”);
(3)质量分数为w2的氨水与$\frac{{w}_{2}}{5}$的氨水等质量混合,所得溶液的密度>ρ2 g•cm-3 (填“>”、“<”或“=”);
(4)如果蒸发溶剂使硫酸的质量分数变为2w1,则所得硫酸的物质的量浓度>2c1(填“>”、“<”或“=”).
 已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,相关数据如表所示.
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,相关数据如表所示.| 溶质的物质的量浓度/mol•L-1 | 溶质的质量分数 | 溶液的密度/g•cm-3 | |
| 硫酸 | c1 | w1 | ρ1 |
| 氨水 | c2 | w2 | ρ2 |
(1)表中硫酸的质量分数w1为$\frac{98{c}_{1}}{1000{ρ}_{1}}$(不写单位,用含c1、ρ1的代数式表示);
(2)物质的量浓度为c1 mol•L-1,质量分数为w1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1,质量分数>$\frac{{w}_{1}}{2}$(填“>”、“<”或“=”);
(3)质量分数为w2的氨水与$\frac{{w}_{2}}{5}$的氨水等质量混合,所得溶液的密度>ρ2 g•cm-3 (填“>”、“<”或“=”);
(4)如果蒸发溶剂使硫酸的质量分数变为2w1,则所得硫酸的物质的量浓度>2c1(填“>”、“<”或“=”).
11.下列关于实验基本操作的叙述正确的是( )
| A. | 使用分液漏斗和容量瓶时,首先要洗净 | |
| B. | 蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体暴沸 | |
| C. | 用蒸发皿进行加热蒸发时,一定要垫石棉网 | |
| D. | 向试管中加液体时,胶头滴管紧贴试管内壁 |
 光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.