题目内容
12.在2L恒容密闭容器中发生如图甲的反应.下列判断正确的是( )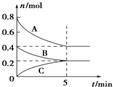
| A. | 5min的时A的转化率为50% | |
| B. | 化学反应方程式为:3A(g)+2B(g)?2C(g) | |
| C. | 降低温度,化学反应速率减小,活化分子百分数不变 | |
| D. | 反应从开始到5min的平均速率v(B)=0.04 mol•L-1•min-1 |
分析 A、根据转化率为$\frac{A的物质的量变化量}{A的起始量}×100%$;
B、由图A、B的物质的量减少,C的物质的量增加,所以A、B是反应物,C是生成物,再结合速率之比等于对应物质的化学计量数之比;
C、降低温度,活化分子百分数降低;
D、根据v=$\frac{△c}{△t}$计算.
解答 解:A、根据转化率为$\frac{A的物质的量变化量}{A的起始量}×100%$=$\frac{0.4}{0.8}×100%$=50%,故A正确;
B、由图A、B的物质的量减少,C的物质的量增加,所以A、B是反应物,C是生成物,A、B、C的物质的量的变化量之比为:0.4:0.2:0.2=2:1:1,所以化学方程式为:2A(g)+B(g)?C(g),故B错误;
C、降低温度,化学反应速率减小,活化分子百分数降低,故C错误;
D、根据v=$\frac{△c}{△t}$=$\frac{\frac{0.2mol}{2L}}{5min}$=0.02 mol•L-1•min-1,故D错误;
故选A.
点评 本题考查了化学平衡图象问题、平衡有关计算等,难度中等,根据图象判断反应物和生成物,结合相关公式计算,注意把握图象中曲线的变化特点.

练习册系列答案
相关题目
2.离子方程式中CO32-+2H+═H2O+CO2↑的CO32-不可能来自下列物质中的( )
| A. | K2CO3 | B. | Na2CO3 | C. | CaCO3 | D. | (NH4)2CO3 |
3.只用一种试剂,可以一次性鉴别NH4Cl、NaCl、Na2SO4三种溶液,这种试剂是( )
| A. | Ba(OH)2溶液 | B. | KCl溶液 | C. | 酚酞溶液 | D. | 盐酸 |
20.下列说法错误的是( )
| A. | 从CH4、NH4+、SO42-为正四面体结构,可推测PH4-、PO43-也为正四面体结构 | |
| B. | 1 mol金刚石晶体中,平均含有2 mol C-C键 | |
| C. | HF、HCl、HBr、HI的热稳定性从左到右依次减弱 | |
| D. | 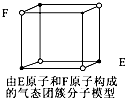 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
7.焙制糕点时,常用到小苏打粉,小苏打的化学式为( )
| A. | NaNO3 | B. | Na2CO3 | C. | NaHCO3 | D. | Na2SO4 |
17.下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是( )
| A. | NaOH溶液中混有Ba(OH)2 (K2SO4溶液) | B. | O2中混有H2(灼热的氧化铜) | ||
| C. | CO2中混有HCl气体 (NaOH溶液) | D. | Cu粉中混有Al粉(稀盐酸) |
4.某酯在稀硫酸中水解得到甲和乙,且甲和乙的相对分子量相等,则该酯可能为( )
| A. | 甲酸甲酯 | B. | 乙酸乙酯 | C. | 甲酸乙酯 | D. | 乙酸甲酯 |
1.下列应用与盐类的水解无关的是( )
| A. | 纯碱溶液可去除油污 | |
| B. | FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 | |
| C. | TiCl4溶于大量水加热制备TiO2 | |
| D. | 保存FeSO4溶液时加入少量铁粉 |