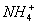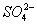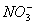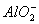��Ŀ����
ij����������ܺ���MgCO3��Al2(SO4)3��Na2SO4Ba(NO3)2��AgNO3��CuSO4�����û�����������ʵ�飬��������ʵ��������ɱ���(���ڿ���ȷ������������Ӧλ��д��ѧʽ���ݲ���ȷ������������Ӧλ����ޡ�)��
(1���������������ˮ�еõ���ɫ��Һ�Ͱ�ɫ������
| �϶����ڵ����� | �϶������ڵ����� | ���� |
(2��ȡ��Һ������ɫ��Ӧ������ʻ�ɫ��
| �϶����ڵ����� | �϶������ڵ����� | ���� |
(3��ȡ��ɫ��������ϡ���ᣬ������ȫ�ܽⲢ�ų����塣
| �϶����ڵ����� | �϶������ڵ����� | ���� |
(4��ͨ������ʵ������ȷ����������__________________��
�𰸣���1��
| �� | CuSO4 | ��Һ��ɫ����CuSO4Ϊ��ɫ |
��2��
| Na2SO4 | �� | Na����ɫ��Ӧ�ʻ�ɫ |
��3��
| MgCO3 | Ba(NO3)2 AgNO3 | MgCO3����HCl������CO2������Ba(NO3)2��AgNO3����Na2SO3��Ӧ�� ����BaSO4��Ag2SO4��������HCl�� |
(4��Al2(SO4)3��
����������1��������Һ��ɫ������CuSO4��һ�������ڣ���ΪCuSO4��ҺΪ��ɫ��MgCO3����ˮ��Al2(SO4)3��Na2SO4��Ba(NO3)2��AgNO3�е�����һ�ַ�Ӧ���ɲ�����ɫ�������������ʲ���ȷ����
(2)������ɫ��Ӧ������ʻ�ɫ��˵��һ����Na�����ڣ���һ����Na2SO4���������ʲ���ȷ����
(3)��ɫ��������ϡ���ᣬ������ȫ�ܽ⣬�ҷų����壬˵������ΪMgCO3��������Na2SO4���ڣ�����Ba(NO3)2��AgNO3�����ܴ��ڣ���Һ���Ƿ���Al2(SO4)3���ܿ϶�
������������������ӵļ���

���ᡢ�����̼���ǻ�ѧʵ����о��г��õļ����ᡣ
��֪�����£�Ka��CH3COOH����1.7��10��5 mol��L��1 ��H2CO3�ĵ��볣��
Ka1��4.2��10��7mol��L��1 �� Ka2��5.6��10��11mol��L��1
(1)�����£����ʵ���Ũ����ͬ������������Һ�� a������������Һb������������Һc��̼������Һd��̼��������Һe����������Һ����PH�ɴ�С��˳���ǣ� ������ţ���
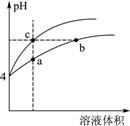 (2)ij�¶��£�pH��Ϊ4������ʹ�����Һ�ֱ��ˮϡ�ͣ���pH����Һ����仯������ͼ��a��b��c�����Ӧ����Һ��ˮ�ĵ���̶��ɴ�С��˳���� ���ô�����Һϡ�����У����и���һ����С���� ��
(2)ij�¶��£�pH��Ϊ4������ʹ�����Һ�ֱ��ˮϡ�ͣ���pH����Һ����仯������ͼ��a��b��c�����Ӧ����Һ��ˮ�ĵ���̶��ɴ�С��˳���� ���ô�����Һϡ�����У����и���һ����С���� ��
a��c(H��) b��c(OH��)
c��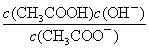 d��
d��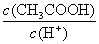
(3)��0.10 mol��L��1NaOHΪ��Һ���ⶨij�����Ũ�ȡ�ȡ20.00 mL����������Һ������ƿ�У����μ�2��3�η�̪��ָʾ������NaOH����Һ���еζ����ظ������ζ�����2��3�Σ���¼�������¡�
| ʵ���� | ����������Һ��Ũ��(mol��L��1) | �ζ����ʱ������������Һ��������(mL) | ������������(mL) |
| 1 | 0.10 | 24.12 | 20.00 |
| 2 | 0.10 | 23. 88 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
�ٵζ��ﵽ�յ�ı�־��___________________________________________��
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ__________________��
����t��ʱ��ijNaOHϡ��Һ��c(H+)=10��a mol��L��1��c(OH��)=10��b mol��L��1��
��֪a+b=12����
�ٸ��¶���ˮ�����ӻ�����Kw= mol2��L��2��
���ڸ��¶��£���100mL0.1 mol��L��1��ϡH2SO4��100mL0.4 mol��L��1��NaOH��Һ��Ϻ���Һ��pH= ��
 CH3OH(g) ��H1����90.7kJ��mol-1
CH3OH(g) ��H1����90.7kJ��mol-1
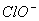 ��CO2��H2O=HClO��
��CO2��H2O=HClO��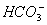
 Mn2����Cl2����2H2O
Mn2����Cl2����2H2O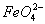 ��3
��3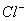 ��H2O��4H��
��H2O��4H��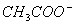 ��H����
��H����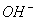 �������ӡ�������������ȷ����( )
�������ӡ�������������ȷ����( )