题目内容
【题目】某兴趣小组查阅资料得知:碘化钠是白色晶体无嗅,味咸而微苦,在空气和水溶液中逐渐析出碘而变黄或棕色。工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下,有关说法不正确的是( )
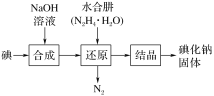
已知:N2H4·H2O在100℃以上分解。
A.已知在合成过程的反应产物中含有NaIO3,若合成过程中消耗了3mol I2,最多能生成NaIO3的物质的量为1 mol
B.上述还原过程中主要的离子方程式为2IO3-+3N2H4·H2O=2I-+3N2+9H2O
C.为了加快反应速率,上述还原反应最好在高温条件下进行
D.工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,因产物是N2和H2O,没有其他副产物,不会引入杂质
【答案】C
【解析】
A. 合成过程的反应产物中含有NaIO3,根据氧化还原反应得失电子守恒规律可知,若合成过程中消耗了3 mol I2,最多能生成 NaIO3 1 mol ,即失去5 mol电子,同时得到5 mol NaI,A项正确;
B. 根据氧化还原及流程图可知上述还原过程中主要的离子方程式为2IO3-+3N2H4·H2O=2I-+3N2+9H2O 或2IO3-+3N2H4=2I-+3N2+6H2O,B项正确;
C. 温度高反应速率快,但水合肼高温易分解,反应温度控制在60~70 ℃比较合适,C项错误;
D. 工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,因产物是N2和H2O,没有其他副产物,不会引入杂质,D项正确;
答案选C。

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目