题目内容
【题目】反应①是制备SiH4的一种方法,利用其副产物可制备相应物质,有关转化关系如下:
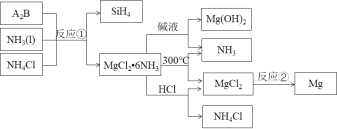
下列说法不正确的是( )
A.A2B的化学式为Mg2Si
B.NH3、NH4Cl可以循环使用
C.反应①中参加反应的NH3和NH4Cl的物质的量之比为1∶1
D.反应②中每生成24gMg转移2mol电子
【答案】C
【解析】
根据化学反应的本质,反应①的产物中出现Si和Mg元素,结合Mg为+2价、Si为-4价,可知A2B应为Mg2Si,与氨气、氯化铵反应生成SiH4和MgCl26NH3,MgCl26NH3加入碱液,可生成Mg(OH)2,MgCl26NH3加热时不稳定,可分解生成氨气,同时生成氯化镁,电解熔融的氯化镁,可生成镁,用于工业冶炼,而MgCl26NH3与盐酸反应,可生成氯化镁、氯化铵,其中氨气、氯化铵可用于反应①而循环使用,以此解答该题。
A.由分析知,A2B应为Mg2Si,故A正确;
B.由分析知,产物氨气、氯化铵可用于反应①而循环使用,故B正确;
C.反应①发生反应的化学方程式为Mg2Si+8NH3+4NH4Cl=SiH4+2MgCl26NH3,则参加反应的NH3和NH4Cl的物质的量之比为2:1,故C错误;
D.反应②中电解MgCl2生成Mg,其中Mg元素从+2价降为0价,则每生成24g(1mol)Mg转移2mol电子,故D正确;
故答案为C。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案【题目】根据下列实验操作和现象所得到的结论正确的是![]()
![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 向足量含KSCN的 | 溶液变黄 | 还原性:Fe2+>Br- |
B | 向2mL浓度为 | 开始出现白色沉淀,后出现黄色沉淀 |
|
C | 取等质量的Al和Fe,分别与足量的稀硫酸反应 | Al产生的氢气多 | 金属性: |
D | 向苯酚浊液中滴加饱和 | 浊液变澄清 | 酸性:苯酚 |
A.AB.B/span>C.CD.D
【题目】我国高铁、航空航天、手机制造等都已经跻身世界一流水平,根据下列材料的应用回答问题。
应用 | “复兴号”高铁车轮 | “鲲龙”水陆两栖飞机零部件 | 华为折叠手机屏幕 |
用到的材料 | 高速钢 | 钛合金、铝合金 | 聚酰亚胺塑料 |
(1)上述材料中属于有机合成材料的是______,属于金属材料的是______(写一种即可)。
(2)飞机外壳用钛合金、铝合金的优点是______。
(3)在对高铁钢轨中的缝隙进行焊接时,常用铝和氧化铁在高温条件下反应生成熔融状态下的铁和另一种氧化物。写出该反应的化学方程式为______,反应基本类型是______。