��Ŀ����
����Ŀ�������¶��£����ܵ���ʵı�����Һ�д��ڳ����ܽ�ƽ�⣬��֪��
���� | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
KSP(25��) | 8.0��10-16 | 2.2��10-20 | 4.0��10-38 |
25��ʱ������CuSO4��FeSO4��Fe2(SO4)3��0.5mol��1L�����Һ�������ϱ����ݶϣ�����˵������ȷ���ǣ� ��
A. ������Һ�м���������ˮ��������pH��3��4����ˣ��ɻ�ô�����CuSO4��Һ
B. ������Һ����μ���NaOH��Һ�����ȿ������ɫ����
C. ����Һ��c(SO42-)��[c(Cu2��)+ c(Fe2��)+c(Fe3��)]��5��4
D. ��pH=5����Һ�У�Fe3�����ܴ�������
���𰸡�A
��������A. ���ɿ�����(NH4)2SO4�����ܻ�ô�����CuSO4��Һ����A����ȷ��B. ������Һ����μ���NaOH��Һ����ʼ����Fe(OH)3ʱpH��С���������ȿ������ɫ��������B��ȷ��C. ����Һ��c(SO42-)=2.5mol/L������Cu2����Fe2����Fe3������ˮ�ⷴӦ��ʹ��c(Cu2��)+c(Fe2��)+c(Fe3��)<2.0mol/L����ˣ�c(SO42-)��[c(Cu2��)+ c(Fe2��)+c(Fe3��)]��5��4����C��ȷ��D. ��pH=5����Һ��c(OH��)=1��10-9mol/L��Fe3������ȫ����ʱ��c(Fe3��)��1��10-5mol/L��c(OH��)��(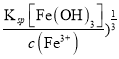 =(
=(![]() <1��10-9mol/L��������pH=5����Һ�У�Fe3�����ܴ������ڣ���D��ȷ����ѡA��
<1��10-9mol/L��������pH=5����Һ�У�Fe3�����ܴ������ڣ���D��ȷ����ѡA��

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�����Ŀ����һ���¶��£�������X������Y��0.32mol����10L�����ܱ������У�������Ӧx(g)+ Y(g) ![]() 2Z(g)AH<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g)AH<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.24 | 0.22 | 0.20 | 0.20 |
����˵����ȷ������ ��
A. ��Ӧǰ2min ��ƽ������ v(Z)=4.0��10-3mol/(L��min)
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv������>v������
C. ���¶��´˷�Ӧ��ƽ�ⳣ��k=1.44
D. �����������䣬�ٳ���0.2molZ��ƽ��ʱX�����������С



