题目内容
(8分)在密闭容器中,使2molN2和6molH2混合发生下列反应:
N2(g)+3H2(g)===2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量_______,密度________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将C(N2)、C(H2)、C(NH3)同时减小一倍,平衡将向______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将_______
(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_______(填“大于”“小于”或“等于”)原来的2倍。
N2(g)+3H2(g)===2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量_______,密度________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将C(N2)、C(H2)、C(NH3)同时减小一倍,平衡将向______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将_______
(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_______(填“大于”“小于”或“等于”)原来的2倍。
(1)1 : 3 ; 1 : 1
(2)变小;不变
(3)逆反应方向
(4)逆反应方向
(5)向左移动,小于
(2)变小;不变
(3)逆反应方向
(4)逆反应方向
(5)向左移动,小于
略

练习册系列答案
相关题目
 还含有碳氢化合物等污染物,下图是汽车尾气转化研究的示意图:表示的是Pt/Al2O3/Ba表面吸附与解吸作用的机理,氮氧
还含有碳氢化合物等污染物,下图是汽车尾气转化研究的示意图:表示的是Pt/Al2O3/Ba表面吸附与解吸作用的机理,氮氧 化物是NO2,碳氢化合物是CxHy
化物是NO2,碳氢化合物是CxHy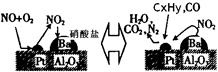
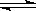 2NO(g) K1=1×10-30 ㈠
2NO(g) K1=1×10-30 ㈠ ①常温下,反应2H2O(g) 2H2(g)
①常温下,反应2H2O(g) 2H2(g) +O2(g) 平衡常数K= ;
+O2(g) 平衡常数K= ; 常温下,NO,H2O,CO2三种化合物分解放出氧气的倾向大小顺序:NO>H2O>CO2
常温下,NO,H2O,CO2三种化合物分解放出氧气的倾向大小顺序:NO>H2O>CO2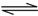 2NH3(g)的△H= 。
2NH3(g)的△H= 。 积分数为 。
积分数为 。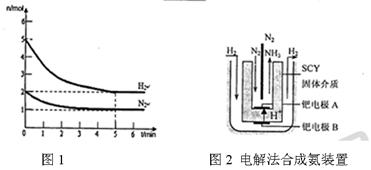
 内外
内外 上发生的电极反应式是 。
上发生的电极反应式是 。  N2O4(g);△H<0,在一定条件下,反应达到平衡后,改变下列条件,再次达到平衡后,容器中气体颜色加深的是( )
N2O4(g);△H<0,在一定条件下,反应达到平衡后,改变下列条件,再次达到平衡后,容器中气体颜色加深的是( ) pC(g)+qD(g);ΔH<0。下列结论中正确的是( )
pC(g)+qD(g);ΔH<0。下列结论中正确的是( ) 增大1倍,此时A的浓度变为原来的0.48 倍,则m+n>p+q
增大1倍,此时A的浓度变为原来的0.48 倍,则m+n>p+q 平衡时,A.B的转化率相等,说明反应开始A.B的物质的量之比为m∶n
平衡时,A.B的转化率相等,说明反应开始A.B的物质的量之比为m∶n