题目内容
5.下列离子方程式正确的是( )| A. | 用氯化铁溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 过氧化钠与水反应制备氧气:Na2O2+2H2O═2N++2OH-+O2↑ | |
| C. | 硫酸亚铁溶液中通氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 用惰性电极电解饱和食盐水:2H++2Cl-═H2↑+Cl2↑ |
分析 A.电荷不守恒;
B.原子个数不守恒;
C.二价铁离子能够被氯气氧化生成三价铁离子;
D.用惰性电极电解饱和食盐水生成氢氧化钠、氯气和水.
解答 解:A.氯化铁溶液腐蚀印刷电路板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.过氧化钠与水反应制备氧气,离子方程式:2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.硫酸亚铁溶液中通氯气,离子方程式:2Fe2++Cl2═2Fe3++2Cl-,故C正确;
D.用惰性电极电解饱和食盐水,离子方程式:2H20+2Cl-═H2↑+Cl2↑+2OH-,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子方程式应遵循客观事实、遵循原子个数电荷数守恒 规律,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
15. A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
(1)将A、E两种元素的元素符号填入下表中正确的位置上.
(2)A、B、C、D、E、F六种元素中非金属性最强的是F(填元素符号),B、D量元素可以组成原子个数比为1:1的离子化合物,写出该离子化合物的电子式: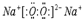 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
 A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.(1)将A、E两种元素的元素符号填入下表中正确的位置上.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ----------------- | |||||||
| 二 | ||||||||
| 三 | ||||||||
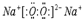 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
16.已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下:下列说法不正确的( )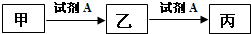
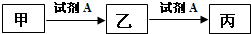
| A. | 若A为硝酸,X为金属元素,则甲与丙反应可生成乙 | |
| B. | 若乙为NaHCO3,则丙一定是CO2 | |
| C. | 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质 | |
| D. | 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
20.下列与物质分类相关的说法正确的是( )
| A. | 只含一种分子的物质一定是纯净物 | |
| B. | 由Na2O2制取O2一定要加入氧化剂 | |
| C. | 金属氧化物一定是碱性氧化物 | |
| D. | 含氧酸受热分解都能生成对应的酸酐和水 |
17.已知重铬酸钾(K2Cr2O7)是一种比高锰酸钾还要强的氧化剂,其溶液中存在如下平衡:2CrO42-(黄色)+2H +?Cr2O72-(橙色)+H2O若要使溶液的橙色加深,下列可采用的方法是( )
| A. | 加入适量稀盐酸 | B. | 加入适量稀硫酸 | ||
| C. | 加入适量烧碱固体 | D. | 加水稀释 |
14.下列关于化学反应与能量的说法正确的是( )
| A. | 中和反应是放热反应 | |
| B. | 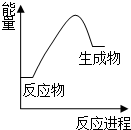 H2燃烧时的能量变化如图所示 | |
| C. | 化学键断裂放出能量 | |
| D. | 反应物总能量与生成物总能量一定相等 |
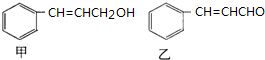
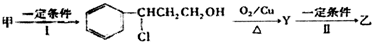
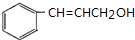 +HCl$\stackrel{一定条件下}{→}$
+HCl$\stackrel{一定条件下}{→}$ ,反应II的反应类型为消去反应.
,反应II的反应类型为消去反应.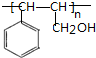 .
.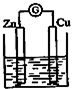 X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题:
X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题: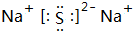 .
.