��Ŀ����
��X��Y��Z��W���ֺ����ᣬ�����Ԫ�ؾ�ΪԪ�����ڱ��еĶ�����Ԫ�أ����ֱ���һ��������X��Y��Z��W��ˮ��Һ���й��ջ��ȣ��йصķ�Ӧ��������ȫ������õ��������±���
�ݴ��ж�����������ȷ���ǣ�������
| ������ | X | Y | Z | W |
| �����������/g | 25.2 | a | 3.1 | 10.5 |
| ������U������/g | 3.2 | / | / | 3.2 |
| ������V������/g | 3.6 | 0.9 | 0.9 | / |
| ��ͬ������Q������/g | 18.4 | 3.2 | b | c |
| A���������a=5.1g |
| B��������Y���� |
| C�����ֺ�����ij���Ԫ�صĻ��ϼ۷ֱ�Ϊ+4��+5 |
| D�����ֺ���������һ����ǿ����ʡ�������������� |
�ڳ����������У������ֽ�������ᡢ̼�ᡢ�����ᡢ�����ᣬ�ֽ���������ֵ������ᣬ�ݴ˿���ȷ��XΪHNO3�����ݲ����������ϵ��ȷ��UΪO2��VΪH2O��QΪNO2���������غ��֪a=0.9g+3.2g=4.1g��b=3.1g-0.9g=2.2g��c=10.5g-3.2g=7.3g�����ɴ˿���ȷ��YΪH2SO3��ZΪH2CO3��WΪHClO������ѡ��D��ȷ��A��B��C����ȷ����ѡD��
�𰸣�D
�𰸣�D

��ϰ��ϵ�д�
�����Ŀ


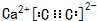

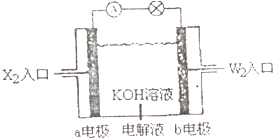 ��X��Y��Z��W���ֶ�����Ԫ�أ�ԭ��������������X�������Ӿ���һ�����ӣ�Z��W�����ڱ��ڴ���ͬһ��������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮Yԭ�ӵ������������Ǵ�����������2������ش�
��X��Y��Z��W���ֶ�����Ԫ�أ�ԭ��������������X�������Ӿ���һ�����ӣ�Z��W�����ڱ��ڴ���ͬһ��������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮Yԭ�ӵ������������Ǵ�����������2������ش�