题目内容
【题目】下图为元素周期表截取的短周期的一部分,即四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是 ( )
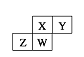
A.原子半径:W>Z>Y>X
B.气态氢化物的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物肯定为强碱
【答案】C
【解析】
元素的结构、位置、性质之间存在必然的联系,据此分析判断。
图中为短周期非稀有气体元素,必为第二、三周期的IIIA、IVA、VA或IVA、VA、VIA或VA、VIA、VIIA族。
A. 据主族元素原子半径的周期性规律,原子半径:Z>W>X>Y,A项错误;
B. 四种元素的非金属性Y>X>W>Z,则气态氢化物的稳定性Y>X>W>Z,B项错误;
C. 从位置关系看,W可能为Si、P、S。若为Si,则其最高正化合价+4、最低负化合价-4,C项正确;
D. Z可能为Al、Si、P,其最高价氧化物的水化物不可能为强碱,D项错误。
本题选C。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】某化学兴趣小组要完成中和热的测定实验。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃玻璃棒、50 mL0.25 mol· L-1稀硫酸、50 mL 0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是:__________________、__________________。
(2)某同学用该装置做实验,因有些操作不规范,造成所测中和热的数值偏低,请分析可能的原因是_________________(用标号字母填写)。
A.测量稀硫酸温度后,温度计没用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C. 量取稀硫酸时仰视计数
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.大烧杯的盖板中间小孔太大了
(3)实验得到表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
假设0.55mol/LNaOH溶液和0.25mol/L硫酸溶液的密度都近似取1g/cm3,中和后所得溶液的比热容c =4.18 J/(g·℃)。则中和热ΔH =_____________ kJ/mol。
(4)如果用60mL0.25mol/L硫酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_________(填:“增多”、“不变”、“减少”),所求中和热_________(填:“相等”、“不相等”)。
(5)若用KOH代替NaOH,对测定结果_______________(填:“有” 或 “无”)影响。![]()
![]()